
分析 向反应后的溶液中滴加NaOH溶液能产生沉淀,当沉淀量最多时,恰好反应时消耗氢氧化钠溶液体积最小,此时溶液中溶质为NaNO3,由原子守恒可知n(NaOH)=n(NaNO3)=n(HNO3)-n(NO),再根据V=$\frac{n}{c}$计算需要氢氧化钠溶液的体积;
解答 解:向反应后的溶液中滴加NaOH溶液能产生沉淀,当沉淀量最多时,恰好反应时消耗氢氧化钠溶液体积最小,此时溶液中溶质为NaNO3,
硝酸的物质的量为0.05L×4mol/L=0.2mol,生成NO的物质的量为$\frac{0.112L}{22.4L/mol}$=0.005mol
由原子守恒可知n(NaOH)=n(NaNO3)=n(HNO3)-n(NO)=0.2mol-0.005mol=0.195mol,
需要氢氧化钠溶液的体积为$\frac{0.195mol}{2mol/L}$=0.0975L,即为97.5mL,
故答案为:97.5.
点评 本题考查化学方程式计算,侧重考查学生分析计算能力,注意利用守恒法计算解答.


科目:高中化学 来源: 题型:解答题
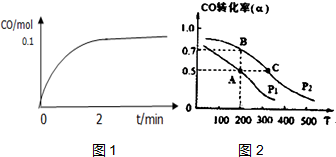 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO (g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO (g)+2H2 (g)?CH3OH (g)△H=-116kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | abc | B. | bcd | C. | abcd | D. | acd |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 炭具有强还原性,高温下能将二氧化硅还原为硅 | |
| B. | Na的金属性比Mg强,可用Na与MgCl2溶液反应制取金属Mg | |
| C. | 光照时乙烷和氯气能发生取代反应,工业上常用该反应生产氯乙烷 | |
| D. | 二氧化锰具有强氧化性,能将双氧水氧化为氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学危险品发生爆炸事故后,人员应该向上风方向撤离 | |
| B. | 含有硫酸的工业废水用硝酸钡处理后再排放有利于减少水体污染 | |
| C. | 用聚苯乙烯代替聚乙烯作食品包装袋,可节约成本,但是不利于人体健康和环保 | |
| D. | “阅兵蓝”的出现说明京津冀实施道路限行和污染企业停工等措施,可以有效地减轻雾霾和保证空气质量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com