
| A、PCl5 |
| B、CCl4 |
| C、NF3 |
| D、N |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、氯化氢气体的摩尔质量等于NA个氯气分子和NA个氢气分子的质量之和 |
| B、常温常压下,1mol SO2约含有6.02×1023个SO2分子 |
| C、18g水中含有1mol H2和16g氧原子 |
| D、62g Na2O溶于水后所得溶液中含有O2-离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
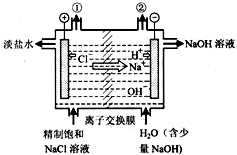
| A、装置中出口①处的物质是氯气,出口②处的物质是氢气 | ||
| B、该离子交换膜只能让阳离子通过,不能让阴离子通过 | ||
C、装置中发生反应的离子方程式为:2Cl-+2H+
| ||
| D、该装置是将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
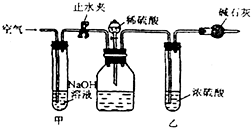
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | V (Na2CO3)/mL | 沉淀情况 | 编号 | 反应温度/℃ | 沉淀情况 | |
| 1 | 2.8 | 多、蓝色 | 1 | 40 | 多、蓝色 | |
| 2 | 2.4 | 多、蓝色 | 2 | 60 | 少、浅绿色 | |
| 3 | 2.0 | 较多、绿色 | 3 | 75 | 较多、绿色 | |
| 4 | 1.6 | 较少、绿色 | 4 | 80 | 较多、绿色(少量褐色) |

| x |
| y |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 ,合成路线如下:
,合成路线如下:

| H2O2 |
 (R-代表烃基)
(R-代表烃基)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、羧酸与醇在强酸的存在下加热,可得到酯 |
| B、乙酸和甲醇发生酯化反应生成甲酸乙酯 |
| C、酯化反应的逆反应是水解反应 |
| D、果类和花草中存在着有芳香气味的低级酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com