
| A. | 石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体 | |
| B. | 高纯度的硅单质广泛用于制作光导纤维 | |
| C. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| D. | 陶瓷是人类应用很早的硅酸盐材料 |
分析 A.石英的成分是二氧化硅,在加热条件下与烧碱、纯碱反应而使坩埚炸裂;
B.光导纤维主要原料为二氧化硅;
C.水晶的主要成分是二氧化硅;
D.陶瓷是传统无机非金属材料,陶瓷是硅酸盐材料.
解答 解:A.烧碱为氢氧化钠、纯碱为碳酸钠,为强碱性盐,二氧化硅为酸性氧化物能够与碱性物质反应,所以不能用瓷坩埚来加热烧碱或纯碱使其熔化,故A错误;
B.高纯度的二氧化硅具有良好的导光性,为制造光导纤维主要原料,故B错误;
C.水泥、玻璃是硅酸盐产品,水晶的主要成分是二氧化硅,故B错误;
D.陶瓷的主要原料是黏土,陶瓷是人类应用很早的硅酸盐材料,故D正确.
故选D.
点评 本题考了硅元素及其化合物知识,掌握硅及其化合物的性质和用途,明确二氧化硅、硅及硅酸盐的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素在人体内具有抗氧化、增强免疫力等功效 | |
| B. | 元素符号为 Sn | |
| C. | 在元素周期表中位于第四周期第ⅣA 族 | |
| D. | 属于金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 奶精能使溴水和酸性KMnO4溶液褪色,其原理相同 | |
| B. | 氢化植物油在稀H2SO4和NaOH溶液中发生水解,所得产物相同 | |
| C. | 白砂糖在人体内水解转化为果糖而被人体吸收 | |
| D. | 奶粉可作为人体所需的一种营养物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
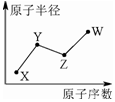 X、Y、Z、W是四种常见的短周期主族元素,其单质都是双原子气体分子.它们原子半径随原子序数的变化如下图所示.已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )
X、Y、Z、W是四种常见的短周期主族元素,其单质都是双原子气体分子.它们原子半径随原子序数的变化如下图所示.已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )| A. | Y、Z、W处于同一周期 | |
| B. | Y、W的最简单氢化物的水溶液能相互反应生成离子化合物 | |
| C. | 非金属性:Y>Z | |
| D. | X、Z、W形成的化合物均为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯与Br2加成:CH2═CHCH3+Br2→CH2BrCH2CH2Br | |
| B. | 甲烷与Cl2发生取代反应:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| C. | 催化裂化:C16H34$→_{△}^{催化剂}$C8H16+C8H18 | |
| D. | 淀粉水解:(C6H10O5)n+nH2O$\stackrel{催化剂}{→}$nC6H12O6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com