
| A. | 一项 | B. | 二项 | C. | 三项 | D. | 四项 |
分析 (1)对于化学平衡加入催化剂会改变反应速率不改变化学平衡;
(2)反应前后气体体积不变的反应增大压强,反应速率增大,化学平衡不变;
(3)化学平衡状态正逆反应速率相同,若平衡移动,正逆反应速率不同,速率发生改变;
(4)两种反应物增加一种会提高另一种转化率,本身转化率减小;
(5)反应前后气体体积不变的反应增大压强,反应速率增大,化学平衡不变;
(6)生成物质量增大小于混合物总质量增大,生成物的质量分数可能降低.
解答 解:(1)对于化学平衡加入催化剂会改变反应速率不改变化学平衡,当条件改变时,平衡不一定会发生移动,故错误;
(2)反应前后气体体积不变的反应增大压强,反应速率增大,化学平衡不变,当速率发生变化时,平衡不一定发生移动,故错误;
(3)化学平衡状态正逆反应速率相同,若平衡移动,正逆反应速率不同,可能正向进行也可能逆向进行,速率一定发生改变,故正确;
(4)两种反应物增加一种会提高另一种转化率,本身转化率减小,当平衡正向移动时,反应物的转化率不一定增大,故错误;
(5)反应前后气体体积不变的反应,增大压强反应速率增大,化学平衡不变,增大体系压强,化学反应速率加快,反应前后气体体积增大的反应,化学平衡逆向移动,增大体系压强,化学反应速率加快,化学平衡不一定正向移动,故错误;
(6)总质量不变,向正反应移动,生成物的质量分数一定增大,若生成物质量增大小于混合物总质量增大,生成物的质量分数可能降低,故错误;
正确的为(3)
故选A.
点评 本题考查化学平衡的影响因素,题目难度中等,注意影响化学平衡移动的因素,解答时注意从勒沙特列原理的角度分析.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Na+、NO3-、MnO4- | B. | Mg2+、Cl-、Al3+、SO42- | ||
| C. | K+、OH-、HCO3-、NO3- | D. | K+、Na+、Fe3+、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水冲洗泄露的浓硫酸 | B. | 将熟石灰撒在泄露的浓硫酸上 | ||
| C. | 将氧化钡撒在泄露的浓硫酸上 | D. | 用土将泄露的浓硫酸掩埋 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
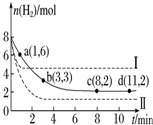 将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标).该反应在8~10min内CO2的平均反应速率是( )
将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标).该反应在8~10min内CO2的平均反应速率是( )| A. | 0.5mol•L-1•min-1. | B. | 0.1mol•L-1•min-1 | ||
| C. | 0 mol•L-1•min-1 | D. | 0.125mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应CaO+H2O═Ca(OH)2能放出大量的热,故可通过原电池实现该反应,并把化学能转化为电能 | |
| B. | 在原电池或电解池装置中,都可实现反应:Cu+2H+═Cu2++H2 | |
| C. | 若原电池的两极是活泼性不同的两种金属,则活泼的金属不一定做负极 | |
| D. | 在钢铁制品上镶嵌锌块构成原电池以防治钢铁生锈,这种防护方法叫外加电源阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO中有少量CaCO3(盐酸) | |
| B. | 氢气中含有少量氯化氢(苛性钠溶液) | |
| C. | 硫酸亚铁溶液中含有少量硫酸铜(铁粉) | |
| D. | CO2中有少量CO(灼热的氧化铜) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com