
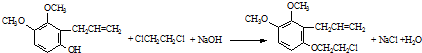 .
. .
.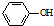 为原料制备
为原料制备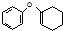 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3 .
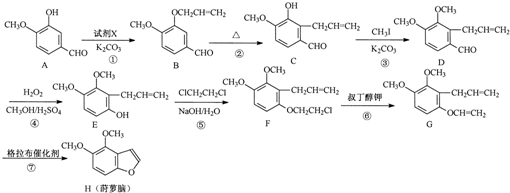
. 分析 (1)由B的结构简式可知,含有的含氧官能团有:醛基、醚键;
(2)试剂X是一溴代烃,对比A、B的结构可知,A中酚羟基中H原子为-CH2CH=CH2取代生成B;对比转化关系中物质的结构判断反应类型;
(3)对比E、F的结构可知,E中酚羟基中H原子为-CH2CH2Cl取代生成F,同时生成HCl,HCl又与氢氧化钠反应生成NaCl与水;
(4)C的一种同分异构体满足下列条件:既能发生银镜反应又能与NaHCO3溶液反应放出CO2,含有-CHO、-COOH;有5种化学环境不同的氢原子且苯环上的一溴代物只有两种,可以是2个不同的取代基处于对位;
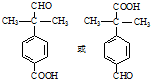
(5)苯酚与氢气发生加成反应生成环己醇,环己醇在浓硫酸、加热条件下发生消去反应生成环己烯,环己烯与溴发生加成反应生成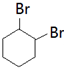 ,由转化关系中反应①、③可知,
,由转化关系中反应①、③可知, 与苯酚发生反应生成
与苯酚发生反应生成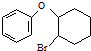 ,再结合转化关系中反应⑥,
,再结合转化关系中反应⑥, 在叔丁醇钾条件下发生消去反应得到
在叔丁醇钾条件下发生消去反应得到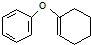 .
.
解答 解:(1)由B的结构简式可知,含有的含氧官能团有:醛基、醚键,故答案为:醛基;醚键;
(2)试剂X是一溴代烃,对比A、B的结构可知,A中酚羟基中H原子为-CH2CH=CH2取代生成B,可知试剂X为BrCH2CH=CH2,对比转化关系中物质的结构,可知反应只有反应⑥中脱下1分子HCl,同时形成碳碳双键,属于消去反应,
故答案为:BrCH2CH=CH2;⑥;
(3)对比E、F的结构可知,E中酚羟基中H原子为-CH2CH2Cl取代生成F,同时生成HCl,HCl又与氢氧化钠反应生成NaCl与水,反应方程式为: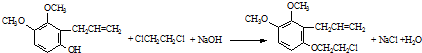 ,
,
故答案为: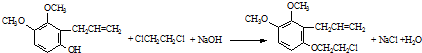 ;
;
(4)C的一种同分异构体满足下列条件:既能发生银镜反应又能与NaHCO3溶液反应放出CO2,含有-CHO、-COOH;有5种化学环境不同的氢原子且苯环上的一溴代物只有两种,可以是2个不同的取代基处于对位,符合条件的同分异构体为: ,
,
故答案为: ;
;
(5)苯酚与氢气发生加成反应生成环己醇,环己醇在浓硫酸、加热条件下发生消去反应生成环己烯,环己烯与溴发生加成反应生成 ,由转化关系中反应①、③可知,
,由转化关系中反应①、③可知, 与苯酚发生反应生成
与苯酚发生反应生成 ,再结合转化关系中反应⑥,
,再结合转化关系中反应⑥, 在叔丁醇钾条件下发生消去反应得到
在叔丁醇钾条件下发生消去反应得到 ,合成路线流程图为:
,合成路线流程图为: ,
,
故答案为: .
.
点评 本题考查有机物的合成、官能团结构、有机反应类型、限制条件同分异构体的书写、合成路线的设计等,需要学生熟练掌握官能团的性质与转化,较好的考查学生阅读获取信息能力、知识迁移应用,是高考热点题型、难度中等.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:多选题
| R | T | |
| X | Y | Z |
| A. | R位于元素周期表中第二周期第VIA族 | |
| B. | 五种元素中原子序数最大的是X | |
| C. | 气态氢化物稳定性:T>Y | |
| D. | Z元素的最高价氧化物对应的水化物的化学式为H2ZO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
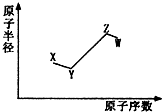 短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )
短周期非金属主族元素X、Y、Z、W,它们的原子半径与原子序数的关系如图所示.其中Z元素原子序数是Y的2倍,原子最外层电子数与X元素原子核外电子数相等,下列说法一定正确的是( )| A. | X和Z、Y和W处于同一主族 | |
| B. | 4种元素形成的各种单质中,Z单质的沸点最高 | |
| C. | W单质与X、Y、Z的最简单氢化物都可以发生反应 | |
| D. | 元素氧化物所对应的水化物酸性:W>Z>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃钢是钢与玻璃纤维形成的复合材料 | |
| B. | 氮氧化物是形成光化学烟雾和酸雨的一个重要原因 | |
| C. | 石油化工废弃物易造成水体富营养化 | |
| D. | 硫酸铵是常用的一种硝态氮肥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(X)>r(Y)>r(Z)>r(W) | |
| B. | X的简单气态氢化物的稳定性比W的弱 | |
| C. | X分别与Y、W形成的化合物中化学键类型相同 | |
| D. | Y的最高价氧化物对应的水化物碱性比Z的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 离子半径:d3+<f- | |
| B. | 原子失电子能力:c>d | |
| C. | 最简单气态氢化物的热稳定性:a<e | |
| D. | b、c两元素可组成既含离子键又含共价键的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物CH3CH(CH3)CH(CH3)CH2CH3名称2,3-二甲基戊烷 | |
| B. | 用新制的Cu(OH)2悬浊液可以鉴别乙酸、乙醇和葡萄糖 | |
| C. | 有机物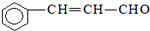 可发生加成反应、氧化反应、还原反应和聚合反应 可发生加成反应、氧化反应、还原反应和聚合反应 | |
| D. | 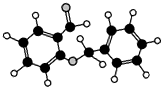 如图所示的有机物分子式为C14H12O2,不能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
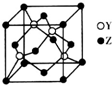 X、Y、Z为前四周期元素,且原子序数依次增大.X与氢元素可形成:H2X、H2X2两种化合物,且在常温下均为液态;Y基态原子的M层电子数是K层的3倍;Z2+的3d轨道中有10个电子.请回答下列问题:
X、Y、Z为前四周期元素,且原子序数依次增大.X与氢元素可形成:H2X、H2X2两种化合物,且在常温下均为液态;Y基态原子的M层电子数是K层的3倍;Z2+的3d轨道中有10个电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
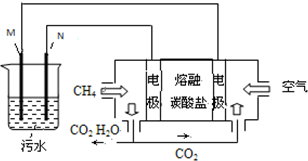 工业废水中常含有一定量的Cr2O72-,会对人类及生态系统产生很大损害,电解法是一种行之有效的除去铬的方法之一.该法用Fe和石墨作电极电解含Cr2O72-的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的.某科研小组利用以上方法处理污水,设计了熔融盐电池和污水电解装置如图所示.
工业废水中常含有一定量的Cr2O72-,会对人类及生态系统产生很大损害,电解法是一种行之有效的除去铬的方法之一.该法用Fe和石墨作电极电解含Cr2O72-的酸性废水,最终将铬转化为Cr(OH)3沉淀,达到净化目的.某科研小组利用以上方法处理污水,设计了熔融盐电池和污水电解装置如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com