
| A. | 2L 0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| B. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 0.1mol 对苯二甲酸中含有双键的数目为0.2NA |
分析 A、在硫酸钾溶液中,阴离子除了硫酸根还有氢氧根;
B、在氢氧化钠溶液中,水的电离被抑制;
C、氢氧燃料电池中正极上放电的是氧气;
D、对二苯甲酸中含2条双键.
解答 解:A、在硫酸钾溶液中,阴离子除了硫酸根还有氢氧根,故溶液中的阴离子所带的电荷数大于2NA个,故A错误;
B、在氢氧化钠溶液中,水的电离被抑制,氢离子全部来自于水的电离,然后根据水电离出的氢氧根和氢离子浓度相同,故此溶液中水电离出氮气氢氧根的个数为10-13NA个,故B错误;
C、氢氧燃料电池中正极上放电的是氧气,故当正极上消耗22.4L氧气即1mol氧气时,转移的电子为4NA个,故C错误;
D、对苯二甲酸中含2条双键,故0.1mol对苯二甲酸中含0.2NA个双键,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 第3列元素种类最多,第14列元素种类也最多 | |
| B. | 第8、9、10三列元素中没有非金属元素 | |
| C. | 从上到下第1列元素的单质熔点逐渐升高,第17列元素的单质熔点逐渐降低 | |
| D. | 只有第2列元素的原子最外层有2个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
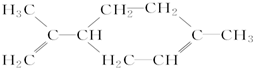
| A. | 柠檬烯的分子式为C10H16,能使溴的四氯化碳溶液褪色 | |
| B. | 柠檬烯分子为非极性分子 | |
| C. | 柠檬烯分子中所有碳原子处于同一个平面上 | |
| D. | 柠檬烯能与酸性高锰酸钾溶液发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
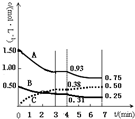 有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )
有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )| A. | 该反应的化学方程式为3A(g)+B(g)═2C(g) | |
| B. | 若将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变 | |
| C. | 若第4 min 时降低温度,到7 min时达到了新的平衡,则此反应的△H<0 | |
| D. | 反应在前3 min的平均反应速率υ(A)=0.31mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L二氯甲烷的分子数约为NA个 | |
| B. | 过氧化钠与水反应时,每生成0.1mol氧气转移的电子数为0.4NA | |
| C. | 电解精炼铜时,若阴极得到的电子数为2NA,则阳极质量减少64g | |
| D. | 3.2g由氧气和臭氧组成的混合物中含有氧原子的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
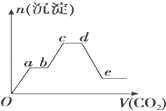 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是( )
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是( )| A. | Oa段反应的化学方程式是Ba(OH)2+CO2═BaCO3↓+H2O | |
| B. | ab段与cd段沉淀质量都不变,但所发生的反应不相同 | |
| C. | bc段反应的离子方程式是:2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- | |
| D. | de段沉淀减少是由于Al(OH)3固体消失的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 L氨气体分解成1 L氮气与3 L氢气吸收92 kJ热量 | |
| B. | 1 mol氮气与3 mol氢气反应生成2 mol液态氨放出的热量小于92 kJ | |
| C. | 25℃和101kPa时,2 molNH3(g)完全分解为1 mol N2(g)和3 mol H2(g )吸热92KJ | |
| D. | 3个氢气分子与1个氮气分子反应生成2个氨气分子放出92 kJ热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com