
分析 (1)根据盖斯定律结合已知热化学方程式来解答;
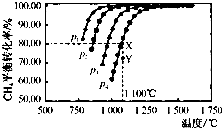
(2)①由图可知,压强一定时,温度越高甲烷的转化率越大,升高温度平衡向正反应进行,据此判断;
②由图可知,温度一定时,甲烷的转化率α(P1)>α(P2)>α(P3)>α(P4),据此结合方程式判断压强对平衡移动的影响进行解答;
③由图可知,压强为P4、1100℃的条件下,到达平衡X点时甲烷的转化率为80%,据此计算甲烷的浓度变化量,利用三段式计算平衡时各组分的平衡浓度,代入平衡常数表达式计算该温度下的平衡常数;
④由于是将Y点平衡体系转化为X点,而通过图象可知,Y平衡体系和X平衡体系所处的温度相同而压强不同,且Y点的压强更大,故由Y点变为X点是通过减小体系压强来实现,据此分析;
(3)①CO2和CH4直接转化成乙酸,由反应物、生成物结合质量守恒定律书写反应方程式;
②Cu2Al2O4溶解在稀硝酸中,发生氧化还原反应生成硝酸铜、硝酸铝、NO和水;
(4)①反应中Fe元素化合价升高,C元素化合价降低,计算生成C的物质的量,结合C元素化合价变价计算转移电子物质的量;
②根据原电池原理,CO2在正极发生还原反应转化为甲烷,注意电解质溶液为碱性.
解答 解:(1)CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=akJ•mol-1 ①
CO(g)+H2O (g)=CO2(g)+H2 (g)△H=bkJ•mol-1 ②
2CO(g)+O2(g)=2CO2(g)△H=ckJ•mol-1 ③
根据盖斯定律,由①+②×2-③×2得,CO2(g)+CH4(g)?2CO(g)+2H2(g)△H=+(a+2b?2c)kJ•mol-1.
故答案为:+(a+2b?2c)KJ/mol;
(2)①由图可知,压强一定时,温度越高甲烷的转化率越大,升高温度平衡向正反应进行,故正反应为吸热反应,即△H>0,故答案为:>;
②由图可知,温度一定时,甲烷的转化率α(P1)>α(P2)>α(P3)>α(P4),该反应正反应是气体体积增大的反应,增大压强平衡向逆反应进行,甲烷的转化率降低,故压强P4>P3>P2>P1,故答案为:P4>P3>P2>P1;
③由图可知,压强为P4、1100℃的条件下,达到平衡X点时甲烷的转化率为80%,甲烷的浓度变化量为0.1mol/L×80%=0.08mol/L,则:
CH4(g)+CO2(g)=2CO(g)+2H2(g),
开始(mol/L):0.1 0.1 0 0
变化(mol/L):0.08 0.08 0.16 0.16
平衡(mol/L):0.02 0.02 0.16 0.16
故该温度下平衡常数k=$\frac{0.1{6}^{2}×0.1{6}^{2}}{0.02×0.02}$=1.64,故答案为:1.64;
④由于是将Y点平衡体系转化为X点,而通过图象可知,Y平衡体系和X平衡体系所处的温度相同而压强不同,且Y点的压强更大,故由Y点变为X点是通过减小体系压强来实现.减小压强后,反应物和生成物的浓度突然变小,故v(正)和v(逆)均立即变小,但由于平衡右移,故反应物的浓度继续减小,而生成物的浓度后来逐渐变大,则v(正)继续变小,v(逆)后来增大,即由Y点变为X点,v(正)一直变小,而v(逆)先变小后增大,故选D;
(3)①CO2和CH4直接转化成乙酸,由反应物、生成物及质量守恒定律可知反应方程式为CO2+CH4$\frac{\underline{\;Cu_{2}Al_{2}O_{4}\;}}{\;}$CH3COOH,故答案为:CO2+CH4$\frac{\underline{\;Cu_{2}Al_{2}O_{4}\;}}{\;}$CH3COOH;
②Cu2Al2O4溶解在稀硝酸中,发生氧化还原反应生成硝酸铜、硝酸铝、NO和水,化学反应为3Cu2Al2O4+32HNO3=6Cu(NO3)2+6Al(NO3)3+2NO↑+16H2O,
故答案为:3Cu2Al2O4+32HNO3=6Cu(NO3)2+6Al(NO3)3+2NO↑+16H2O;
(4)①由方程式可知,每生成1mol Fe3O4时生成0.5molC,C元素化合价由+4价降低为0价,故转移电子为0.5mol×4=2mol,故答案为:2;
②CO2在正极发生还原反应转化为甲烷,电极反应为:CO2+8e-+6H2O=CH4+8OH-,阳极上是氢氧根离子失电子的氧化反应,产生氧气,总的电解原理方程式为:CO2+2H2O$\frac{\underline{\;通电\;}}{\;}$CH4+2O2,故答案为:正;CO2+2H2O$\frac{\underline{\;通电\;}}{\;}$CH4+2O2
点评 本题主要考查盖斯定律、影响化学反应速率和平衡的因素以及原电池原理的运用等知识,综合性较强,是高考的常见题型.


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 在101 k Pa时,1 mol C与适量O2反应生成1mol CO时,放出110.5 kJ热 量,则C的燃烧热为110.5 kJ/mol | |
| B. | 在10l k Pa时l mol H2完全燃烧生成液态水放出285.8 kJ热量,H2燃烧热为-285.8kJ/mol | |
| C. | 鉴定HCl和NaOH反应的中和热时,每次实验均应测量3个温度即盐酸起始温度、NaOH起始温度和反应后终止温度 | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3KJ/mol,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水时,阴极的电极反应式为 2Cl--2e-═Cl2↑ | |
| B. | 放电时,铅蓄电池中硫酸浓度不断减小 | |
| C. | 氢氧燃料电池中,当电路上有1mol 电子通过时,则正极上消耗氧气为5.6L | |
| D. | 以锌片、铜片、稀硫酸组成原电池,当溶液中通过0.2mol电子时,负极减轻6.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①=④>③=② | B. | ④=①>③>② | C. | ①>④>③>② | D. | ④>①=③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
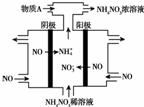 NH4NO3主要用作肥料、军用炸药、冷冻剂、制造笑气等.
NH4NO3主要用作肥料、军用炸药、冷冻剂、制造笑气等.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com