
”¾ĢāÄæ”æĻĀĮŠĪļÖŹµÄ×Ŗ»ÆŌŚøų¶ØĢõ¼žĻĀ²»ÄÜŹµĻֵďĒ( )
A.NH3![]() NO
NO![]() HNO3
HNO3
B.ÅØŃĪĖį![]() Cl2
Cl2![]() ĘÆ°×·Ū
ĘÆ°×·Ū
C.Al2O3![]() AlCl3(aq)
AlCl3(aq) ![]() ĪŽĖ®AlCl3
ĪŽĖ®AlCl3
D.ĘĻĢŃĢĒ![]() C2H5OH
C2H5OH![]() CH3CHO
CH3CHO
”¾“š°ø”æC
”¾½āĪö”æ
°±ĘųµÄ“ß»ÆŃõ»Æ»įÉś³ÉŅ»Ńõ»ÆµŖ£¬Ņ»Ńõ»ÆµŖŗĶŃõĘųÓėĖ®·“Ó¦µĆµ½ĻõĖį£»ÅØŃĪĖįÓė¶žŃõ»ÆĆĢ·“Ӧɜ³ÉĀČĘų”¢ĀČĘųÓėŹÆ»ŅČ鷓Ӧɜ³É“ĪĀČĖįøĘŗĶĀČ»ÆøĘ£»ĀČ»ÆĀĮČÜŅŗŹÜČČĖ®½āÉś³ÉĒāŃõ»ÆĀĮ£»ĘĻĢŃĢĒŌŚ¾Ę»ÆĆøµÄ×÷ÓĆĻĀÉś³ÉŅŅ“¼”¢ŅŅ“¼“ß»ÆŃõ»ÆÉś³ÉŅŅČ©”£
A”¢°±ĘųŌŚ“߻ƼĮ¼ÓČČĢõ¼žĻĀÓėŃõĘų·“Ӧɜ³ÉNO£¬NOŗĶŃõĘųÓėĖ®·“Ó¦µĆµ½ĻõĖį£¬ĪļÖŹµÄ×Ŗ»ÆŌŚøų¶ØĢõ¼žĻĀÄÜŹµĻÖ£¬¹ŹAÕżČ·£»
B”¢ÅØŃĪĖįÓė¶žŃõ»ÆĆĢŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³ÉĀČ»ÆĆĢ”¢Ė®ŗĶĀČĘų£¬ĀČĘųÓėŹÆ»ŅČ鷓Ӧɜ³É“ĪĀČĖįøĘŗĶĀČ»ÆøĘ£¬¼“Éś³ÉĘÆ°×·Ū£¬ĪļÖŹµÄ×Ŗ»ÆŌŚøų¶ØĢõ¼žĻĀÄÜŹµĻÖ£¬¹ŹBÕżČ·£»
C”¢Al2O3ÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆĀĮŗĶĖ®£¬ĀČ»ÆĀĮČÜŅŗŹÜČČĖ®½āÉś³ÉĒāŃõ»ÆĀĮ£¬µĆ²»µ½ĪŽĖ®ĀČ»ÆĀĮ£¬¹ŹC“ķĪó£»
D”¢ĘĻĢŃĢĒŌŚ¾Ę»ÆĆøµÄ×÷ÓĆĻĀÉś³ÉŅŅ“¼”¢ŅŅ“¼ÓėŃõĘųŌŚ“߻ƼĮ¼ÓČČĢõ¼žĻė·“Ӧɜ³ÉŅŅČ©£¬ĪļÖŹµÄ×Ŗ»ÆŌŚøų¶ØĢõ¼žĻĀÄÜŹµĻÖ£¬¹ŹDÕżČ·”£
“š°øŃ”C”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ±ķŹ¾¶ŌÓ¦»Æѧ·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A.ĀČĘųČÜÓŚĖ®£ŗCl2£«H2O![]() H£«£«Cl££«HClO
H£«£«Cl££«HClO
B.MnO2ÓėÅØŃĪĖį·“Ó¦ÖĘCl2£ŗMnO2+4HCl![]() Mn2£«+2Cl£+Cl2”ü+2H2O
Mn2£«+2Cl£+Cl2”ü+2H2O
C.Na2O2ČÜÓŚĖ®²śÉśO2£ŗNa2O2£«H2O£½2Na£«£«2OH££«O2”ü
D.ĻņNaHCO3ČÜŅŗÖŠ¼Ó¹żĮæ³ĪĒåŹÆ»ŅĖ®£ŗ2HCO£«Ca2£«£«2OH£=CaCO3”ż£«CO![]() £«2H2O
£«2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÖŠ¹ś»Æѧ¼ŅŃŠ¾æµÄŅ»ÖÖŠĀŠĶø“ŗĻ¹ā“߻ƼĮ[Ģ¼ÄÉĆ×µć(CQDs)/µŖ»ÆĢ¼(C3N4)ÄÉĆ×ø“ŗĻĪļ]æÉŅŌĄūÓĆĢ«Ńō¹āŹµĻÖøߊ§·Ö½āĖ®£¬ĘäŌĄķČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
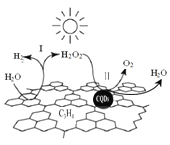
A. C3N4ÖŠCµÄ»ÆŗĻ¼ŪĪŖ -4
B. ·“Ó¦µÄĮ½øö½×¶Ī¾łĪŖĪüČČ¹ż³Ģ
C. ½×¶Ī¢ņÖŠ£¬H2O2¼ČŹĒŃõ»Æ¼Į£¬ÓÖŹĒ»¹Ō¼Į
D. ĶعżøĆ·“Ó¦£¬ŹµĻÖĮĖ»ÆѧÄÜĻņĢ«ŃōÄܵÄ×Ŗ»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
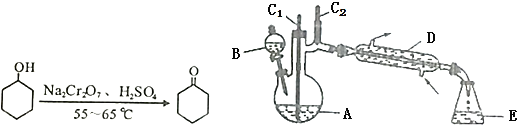
”¾ĢāÄæ”æŹµŃéŹŅæÉĄūÓĆ»·¼ŗ“¼µÄŃõ»Æ·“Ó¦Öʱø»·¼ŗĶŖ£¬·“Ó¦ŌĄķŗĶŹµŃé×°ÖĆ(²æ·Ö¼Š³Ö×°ÖĆĀŌČ„)ČēĻĀ£ŗ
ÓŠ¹ŲĪļÖŹµÄĪļĄķŠŌÖŹ¼ū±ķ”£
ĪļÖŹ | ·Šµć(”ę) | ĆܶČ(g/cm3£¬20”ę) | ČܽāŠŌ |
»·¼ŗ“¼ | 161.1(97.8)* | 0.96 | ÄÜČÜÓŚĖ®ŗĶĆŃ |
»·¼ŗĶŖ | 155.6(95.0)* | 0.95 | Ī¢ČÜÓŚĖ®£¬ÄÜČÜÓŚĆŃ |
Ė® | 100.0 | 1.0 |
*ĄØŗÅÖŠµÄŹż¾Ż±ķŹ¾øĆÓŠ»śĪļÓėĖ®ŠĪ³ÉµÄ¾ßÓŠ¹Ģ¶Ø×é³ÉµÄ»ģŗĻĪļµÄ·Šµć”£
ŹµŃéÖŠĶعż×°ÖĆB½«ĖįŠŌNa2Cr2O7ČÜŅŗ¼Óµ½Ź¢ÓŠ10mL»·¼ŗ“¼µÄAÖŠ£¬ŌŚ55”«65”ę½ųŠŠ·“Ó¦”£·“Ó¦Ķź³Éŗ󣬼ÓČėŹŹĮæĖ®£¬ÕōĮó£¬ŹÕ¼Æ95”«100”ęµÄĮó·Ö£¬µĆµ½Ö÷ŅŖŗ¬»·¼ŗĶŖ“ÖĘ·ŗĶĖ®µÄ»ģŗĻĪļ”£
(1)ŅĒĘ÷DµÄĆū³ĘĪŖ_____”£
(2)¢ŁµĪ¼ÓĖįŠŌNa2Cr2O7ČÜŅŗŹ±·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______________£»(![]() ±»»¹ŌĪŖCr3+)
±»»¹ŌĪŖCr3+)
¢ŚÕōĮó²»ÄÜ·ÖĄė»·¼ŗĶŖŗĶĖ®µÄŌŅņŹĒ_____”£
(3)»·¼ŗĶŖŠčŅŖ¾¹żŅŌĻĀ²Ł×÷Ģį“æ£ŗ
a.ĶłŅŗĢåÖŠ¼ÓČėNaCl¹ĢĢåÖĮ±„ŗĶ£¬¾²ÖĆ£¬·ÖŅŗ
b.Ė®²ćÓĆŅŅĆŃ(ŅŅĆŃ·Šµć34.6”ę£¬Ņ×Č¼ÉÕ)ŻĶČ”£¬ŻĶČ”Ņŗ²¢ČėÓŠ»ś²ć
c.¼ÓČėĪŽĖ®MgSO4¹ĢĢ壬³żČ„ÓŠ»śĪļÖŠÉŁĮæµÄĖ®
d.¹żĀĖ
e.ÕōĮ󔢳żČ„ŅŅĆŃŗó£¬ŹÕ¼Æ151”«156”ęĮó·Ö
¢ŁbÖŠĖ®²ćÓĆŅŅĆŃŻĶČ”µÄÄæµÄŹĒ_____£»
¢ŚÉĻŹö²Ł×÷a”¢dÖŠŹ¹ÓĆµÄ²£Į§ŅĒĘ÷³żÉÕ±”¢²£Į§°ōĶā£¬»¹ŠčŅŖµÄ²£Į§ŅĒĘ÷ÓŠ____”¢___£¬²Ł×÷aÖŠ£¬¼ÓČėNaCl¹ĢĢåµÄ×÷ÓĆŹĒ_____”£
(4)»Öø“ÖĮŹŅĪĀŹ±£¬·ÖĄėµĆµ½“æ²śĘ·Ģå»żĪŖ8mL£¬Ōņ»·¼ŗĶŖµÄ²śĀŹĪŖ____”£(±£Įō3Ī»ÓŠŠ§Źż×Ö)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµē½ā¾«Į¶ĶµÄŃō¼«ÄąÖŠÖ÷ŅŖŗ¬Ag”¢AuµČ¹óÖŲ½šŹō”£ŅŌĻĀŹĒ“Ó¾«Į¶ĶµÄŃō¼«ÄąÖŠ»ŲŹÕŅų”¢½šµÄĮ÷³ĢĶ¼£ŗ
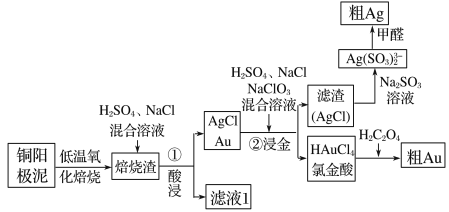
(1)ĀČ½šĖį(HAuCl4)ÖŠµÄAuµÄ»ÆŗĻ¼ŪĪŖ________”£
(2)ĶŃō¼«ÄąŃõ»ÆŹ±£¬²ÉÓĆ”°µĶĪĀ±ŗÉÕ”±¶ų²»²ÉÓĆ”°øßĪĀ±ŗÉÕ”±µÄŌŅņŹĒ_____________________”£
(3)”°±ŗÉÕŌü”±ŌŚ”°¢ŁĖį½ž”±Ź±·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______________________________________”£
(4)”°¢Ś½ž½š”±·“Ó¦ÖŠ£¬H2SO4µÄ×÷ÓĆĪŖ___________________________________________£¬øĆ²½ÖčµÄ·ÖĄė²Ł×÷ÖŠ£¬ŠčŅŖ¶ŌĖłµĆµÄAgCl½ųŠŠĖ®Ļ“”£¼ņŹöČēŗĪÅŠ¶ĻAgClŅŃ¾Ļ“µÓøɾ»£æ _____________________________________________________”£
(5)ĀČ½šĖį(HAuCl4)ŌŚpHĪŖ2”«3µÄĢõ¼žĻĀ±»²ŻĖį»¹ŌĪŖAu£¬Ķ¬Ź±·Å³ö¶žŃõ»ÆĢ¼ĘųĢ壬ŌņøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____________________________________________________”£
(6)¼×Č©»¹Ō·Ø³Į»żŅų£¬Ķس£ŹĒŌŚ½Į°čĻĀÓŚŹŅĪĀ¼°Čõ¼īŠŌĢõ¼žĻĀ½ųŠŠ£¬¼×Č©±»Ńõ»ÆĪŖĢ¼ĖįĒāøłĄė×Ó£¬ŌņøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ___________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£¼ūÓŠ»ś·“Ó¦ĄąŠĶÓŠ£ŗ¢ŁČ”“ś·“Ó¦”¢¢Ś¼Ó³É·“Ó¦”¢¢ŪĻūČ„·“Ó¦”¢¢Üõ„»Æ·“Ó¦”¢¢Ż¼Ó¾Ū·“Ó¦”¢¢ŽŃõ»Æ·“Ó¦”¢¢ß»¹Ō·“Ó¦£¬ĘäÖŠÄÜŌŚÓŠ»śĪļÖŠŅżČėōĒ»łµÄ·“Ó¦ĄąŠĶŹĒ
A. ¢Ł¢Ś¢ŪB. ¢Ł¢Ś¢ßC. ¢Ż¢Ž¢ßD. ¢Ū¢Ü¢Ž
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬ŌŚ3øöĢå»ż¾łĪŖ1.0 LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ·“Ó¦2H2(g)+CO(g)![]() CH3OH(g) “ļµ½Ę½ŗā”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
CH3OH(g) “ļµ½Ę½ŗā”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. øĆ·“Ó¦µÄÕż·“Ó¦·ÅČČ
B. “ļµ½Ę½ŗāŹ±£¬ČŻĘ÷¢ńÖŠ·“Ó¦Īļ×Ŗ»ÆĀŹ±ČČŻĘ÷¢ņÖŠµÄ“ó
C. “ļµ½Ę½ŗāŹ±£¬ČŻĘ÷¢ņÖŠc(H2)“óÓŚČŻĘ÷¢óÖŠc(H2)µÄĮ½±¶
D. “ļµ½Ę½ŗāŹ±£¬ČŻĘ÷¢óÖŠµÄÕż·“Ó¦ĖŁĀŹ±ČČŻĘ÷¢ńÖŠµÄ“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ŲÓŚ·“Ó¦¹ż³ĢÖŠµÄĻČŗóĖ³Šņ£¬ĻĀĮŠĘĄ¼ŪÕżČ·µÄŹĒ
A.ĻņÅØ¶Č¶¼ĪŖ0.1mol/LµÄFeCl3ŗĶCuCl2¼ÓČėĢś·Ū£¬ČÜÖŹCuCl2Ź×ĻČÓėĢś·Ū·“Ó¦
B.Ļņ¹żĮæµÄBa(OH)2ČÜŅŗÖŠµĪ¼ÓÉŁĮæµÄKAl(SO4)2ČÜŅŗ£¬æŖŹ¼Ć»ÓŠ°×É«³ĮµķÉś³É
C.ĻņÅØ¶Č¶¼ĪŖ0.1mol/L µÄNa2CO3ŗĶNaOHµÄ»ģŗĻČÜŅŗĶØČėCO2ĘųĢ壬NaOHŹ×ĻČ·“Ó¦
D.ĻņÅضČĪŖ0.1mol/LµÄFeCl3ČÜŅŗÖŠ£¬¼ÓČėÖŹĮæĻąĶ¬”¢æÅĮ£“óŠ”ĻąĶ¬µÄĢśŗĶĶ£¬Ķµ„ÖŹŹ×ĻČ²Ī¼Ó·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹Ų°±»ņļ§ŃĪµÄĖµ·Ø²»ÕżČ·µÄŹĒ
A. æÉÓĆŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½¼ģŃé°±Ęų
B. ÓĆŃĪĖįµĪ¶Ø°±Ė®£¬µ±ČÜŅŗ³ŹÖŠŠŌŹ±£¬c(NH4+) = c(Cl)
C. NH3ŹōÓŚČõµē½āÖŹ
D. ³£ĪĀŹ±£¬0.1 mol”¤L1NH4ClČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬![]() µÄÖµ²»±ä
µÄÖµ²»±ä
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com