
分析 (1)CCl4从碘水中萃取碘并用分液漏斗分离两种溶液,操作为查漏→装液→振荡→静置→分液;
(2)E操作旋开活塞,分离下层液体,不能使上层液体流出;
(3)(G)步骤可使分液漏斗与外界相通;
(4)碘在水、四氯化碳中的溶解性不同.
解答 解:(1)CCl4从碘水中萃取碘并用分液漏斗分离两种溶液,操作为查漏→装液→振荡→静置→分液,则步骤为C→B→D→A→G→H→E→F,
故答案为:C;B;D;H;
(2)旋开活塞,分离下层液体,应使漏斗下端管口紧靠烧杯内壁,及时关闭活塞,不要让上层液体流出;
故答案为:使分液漏斗下端颈紧靠烧杯内壁,及时关闭活塞,不让上层液体流出;
(3)(G)步骤可使分液漏斗与外界相通,目的为操作时漏斗里液体能够流出;
故答案为:操作时漏斗里液体能够流出;
(4)选用CCl4从碘水中萃取碘的原因是CCl4与水不互溶;而且碘在CCl4中的溶解度比在水中的大得多,
故答案为:CCl4与水不互溶,而且碘在CCl4中的溶解度比在水中的大得多.
点评 本题考查了分液的步骤和萃取剂的选择,难度不大,选择萃取剂紧扣萃取剂的选择标准判断即可,侧重于考查学生对基础知识的应用能力.


科目:高中化学 来源:2016-2017学年四川省高二上教学质检化学试卷(解析版) 题型:填空题
M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中p轨道电子数是s轨道电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,该化合物有漂白性,能使品红溶液褪色,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)Z原子的价电子排布式是 ,X和Y中电负性较大的是 (填元素符号)。
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是 。
(3)X与M形成的XM3分子的空间构型是 ,中心原子的杂化轨道类型 为 。
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如下图所示,则图中黑球代表的离是____________(填离子符号)。
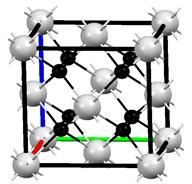
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:选择题
相同温度下等物质的量浓度的下列溶液中,pH值最小的是( )
A.NH4Cl B.NH4HCO3 C.NH4HSO4 D.(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有自发进行的化学反应都是放热反应 | |
| B. | 一定温度下冰转化为水是自发的化学反应 | |
| C. | 由焓判据和熵判据组合而成的复合判据,将更适合于所有的过程 | |
| D. | 同一物质的固液气三种状态的熵值相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
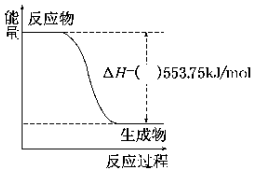 广州亚运会“潮流”火炬采用具有广州民间特色的象牙雕镂空工艺,以水的和谐与火的激情交相凝聚为理念,寄托了亚洲人民共同推进和平与发展的期望.火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:
广州亚运会“潮流”火炬采用具有广州民间特色的象牙雕镂空工艺,以水的和谐与火的激情交相凝聚为理念,寄托了亚洲人民共同推进和平与发展的期望.火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在Fe(OH)3胶体中加入HI溶液:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 标准状况下将112ml氯气通入6ml 1mol/L的碘化亚铁溶液中3Cl2+2Fe2++4I-═6Cl-+2Fe3++2I2 | |
| C. | 向澄清石灰水中加入足量NaHCO3溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| D. | 用H2O2和H2SO4的混合溶液蚀刻铜:Cu+H2O2+2H+═Cu2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 L | B. | 0.1 L | C. | 0.2 L | D. | 1 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{2}$L | B. | $\frac{a}{3}$L | C. | $\frac{a}{4}$L | D. | $\frac{a}{5}$L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com