
(6分,每空3分)完成下列填空:
(1)2g碳与适量水蒸气反应生成CO和H2,需吸收21.80kJ热量,此反应的热化学方程式为________________________________________。
(2)已知 CH4(g)+2O2(g)="=" CO2(g)+2H2O(l);ΔH=-Q1kJ·mol-1 ,
2H2(g)+ O2(g) =2H2O(g);△H2=-Q2 kJ·mol-1,
2H2(g)+ O2(g) =2H2O(l);△H2=-Q3 kJ·mol-1。
常温下,取体积比3∶2的甲烷和氢气的混合气体22.4L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为_________________。
(总计6分)
(1)C(s) + H2O(g) ="=" CO(g) + H2(g) △H=130.80 kJ/mol (3分)
(2)(0.6Q1 + 0.2Q3) kJ (3分)
【解析】
试题分析:(1)热化学方程式中的化学计量数表示的是物质的量,质量要转化为物质的量,热量的变化也要随着改变,故热化学方程式为C(s) + H2O(g) ="=" CO(g) + H2(g) △H=130.80 kJ/mol。(2)燃烧后恢复至室温时水的状态是液态,第二个热化学方程式不用。3∶2的甲烷和氢气的混合气体22.4L(标准状况下),经过计算,甲烷和氢气的物质的量分别为0.6mol、0.4mol。分别带入热化学方程式进行计算的放出的总热量为(0.6Q1 + 0.2Q3) kJ。
考点:热化学方程式的书写反应热的计算
点评:本题考查热化学方程式的书写和根据热化学方程式计算反应热,难度不大,注意根据水的状态选择相应的热化学方程式计算反应热。


科目:高中化学 来源:2012-2013学年湖北省武汉市重点中学高二上学期期中考试化学试卷(带解析) 题型:填空题
(6分,每空3分)完成下列填空:
(1)2g碳与适量水蒸气反应生成CO和H2,需吸收21.80kJ热量,此反应的热化学方程式为________________________________________。
(2)已知 CH4(g)+2O2(g)="=" CO2(g)+2H2O(l);ΔH=-Q1kJ·mol-1 ,
2H2(g)+ O2(g) =2H2O(g);△H2=-Q2 kJ·mol-1,
2H2(g)+ O2(g) =2H2O(l);△H2=-Q3 kJ·mol-1。
常温下,取体积比3∶2的甲烷和氢气的混合气体22.4L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为_________________。
查看答案和解析>>
科目:高中化学 来源:2010年甘肃省高二第二学期期末考试化学试题 题型:填空题
(12分,每空3分).
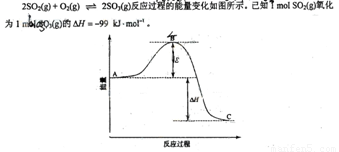
请回答下列问题:
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。
该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(2)图中△H= KJ·mol-1;
查看答案和解析>>
科目:高中化学 来源: 题型:
(6分,每空3分)把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s)+O2(g)===CO2(g);ΔH1<0 ①
途径Ⅱ 先制成水煤气:
C(s)+H2O(g)===CO(g)+H2(g);ΔH2>0 ②
再以水煤气为燃料:
2CO(g)+O2(g)===2CO2(g);ΔH3<0 ③
2H2 (g)+O2(g)===2H2O(g);ΔH4<0 ④
请回答下列问题:
(1)途径Ⅰ放出的热量___ __(填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)ΔH1、ΔH2、ΔH3、ΔH4的数学关系式是__ ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(6分,每空3分)从NO3-、SO42-、H+、Cu2+、Ba2+、Ag+、Cl-等离子中选出适当的离子组成电解质,采用惰性电极对其溶液进行电解。若两极分别放出气体,且体积比为1∶1,电解质的化学式可能是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com