
| A、若C(H+)>C(OH-),则m=n | ||
| B、若C(NH4+)>C(Cl-),则m>n | ||
C、若混合溶液中,C(H+)=
| ||
| D、若C (NH4+)>C(Cl-),则m<n |
| Kw |
| Kw |


科目:高中化学 来源: 题型:
| 名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 | 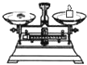 | 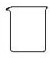 |  |  |  |  |
| 序号 | a | b | c | d | e | f |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三者对应的氧化物均为酸性氧化物 |
| B、加热条件下,浓硝酸可与碳、硫单质发生反应 |
| C、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,向饱和AgCl水溶液中加入盐酸,Ksp值变小 |
| B、25℃时,向CaCO3饱和溶液通入CO2,有沉淀生成 |
| C、25℃时,向CaCl2溶液中通入SO2,有白色沉淀生成 |
| D、25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | U | V | W | X | Y | Z |
| 原子半径/nm | 0.037 | 0.157 | 0.066 | 0.070 | 0.077 | 0.143 |
| 主要化合价 | +1 | +1 | -2 | -3+5 | +2+4 | +3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶上标有温度、浓度、容积和压强 |
| B、如果容量瓶内有少量蒸馏水,必须先对容量瓶进行烘干 |
| C、将所需的氢氧化钠固体倒入到容量瓶中溶解 |
| D、定容时若俯视刻度线观察液面,会使所配制的NaOH 溶液的浓度偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入氢氧化钠溶液并加热,产生气体能使湿润的红色石蕊试纸变蓝,一定有NH4+ |
| B、检验SO2中是否混有CO2,将气体通过澄清的石灰水变浑浊,则说明一定含CO2 |
| C、铝比铁活泼,所以铝比铁更容易被腐蚀 |
| D、正常雨水pH等于7,酸雨的pH小于7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com