
| A. | 酸性氧化物:CO、NO2、SO3、H2O | |
| B. | 碱性氧化物:Na2O、CaO、Mn2O7、Na2O2 | |
| C. | 碱:NaOH、Cu2(OH)2CO3、Ba(OH)2、NH3•H2O | |
| D. | 酸:HN3、CH3COOH、H2S、H3PO2 |
分析 A.酸性氧化物是指和碱反应生成盐和水的氧化物;
B.碱性氧化物是指和酸反应生成沿河水的氧化物;
C.水溶液中电离出的阴离子全部是氢氧根离子的化合物;
D.酸是水溶液中电离出的阳离子全部是氢离子的化合物.
解答 解:A.酸性氧化物是指和碱反应生成盐和水的氧化物,SO3是酸性氧化物,CO、H2O为不成盐氧化物,NO2和碱反应发生的是氧化还原反应不是酸性氧化物,故A错误;
B.碱性氧化物是指和酸反应生成沿河水的氧化物,Na2O、CaO是碱性氧化物、Mn2O7是酸性氧化物,Na2O2和酸反应生成盐、水和氧气不是碱性氧化物,故B错误;
C.水溶液中电离出的阴离子全部是氢氧根离子的化合物,NaOH、Ba(OH)2、NH3•H2O是碱,Cu2(OH)2CO3是盐,故C错误;
D.酸是水溶液中电离出的阳离子全部是氢离子的化合物,HN3、CH3COOH、H2S、H3PO2,水溶液中电离出的阳离子全市氢离子,都属于酸,故D正确;
故选D.
点评 本题考查了物质分类、物质组成、物质名称等知识点,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、Al3+、Cl- | B. | Na+、Fe3+、OH-、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | Ca2+、Mg2+、HCO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其它分散系的本质特征是分散质的微粒直径在10-9-10-7m之间 | |
| B. | FeCl3溶液是电中性的,Fe(OH)3胶体带正电荷 | |
| C. | 胶体的分散质能通过滤纸空隙 | |
| D. | 树林中晨曦的阳光光束现象与丁达尔现象有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ | |
| B. | CO2通入石灰乳中:CO2+Ca2++2OH-═CaCO3↓+H2O | |
| C. | 铁屑溶于稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 向FeBr2溶液中通入足量的Cl2:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
下列反应中,属于氧化还原反应的是
A.CaCO3+2HCl=CaCl2+H2O+CO2↑
B.CaO+H2O=Ca(OH)2
C.CaCO3=CaO+CO2↑
D.2H2O2=2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏卫一高一上10月月考化学a卷(解析版) 题型:选择题
甲、乙、丙、丁分别是Na2CO3、AgNO3、BaCl2、盐酸四种无色溶液中的一种,它们两两反应后的现象如下:甲+乙→沉淀;甲+丙→沉淀;乙+丙→沉淀;丙十丁→沉淀;乙+丁→无色无味气体。则甲、乙、丙、丁四种溶液依次是
A.BaCl2、Na2CO3、盐酸、AgNO3
B.Na2CO3、盐酸、AgNO3、BaCl2
C.BaCl2、Na2CO3、AgNO3、盐酸
D.AgNO3、盐酸、BaCl2、Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
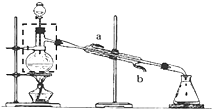 某实验小组用无水乙醇、乙酸与浓硫酸制取乙酸乙酯并提纯,已知乙醇可以和氯化钙反应生成微溶的CaCl2•6C2H5OH.请回答下列问题:
某实验小组用无水乙醇、乙酸与浓硫酸制取乙酸乙酯并提纯,已知乙醇可以和氯化钙反应生成微溶的CaCl2•6C2H5OH.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com