
下列叙述正确的是( )
A.某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b
B.在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7
C.1.0×10—3mol·L— 1盐酸的pH=3.0,1.0×10—8mol·L—1盐酸的pH=8.0
1盐酸的pH=3.0,1.0×10—8mol·L—1盐酸的pH=8.0
D.将pH=2的某酸溶液和pH=12的KOH溶液等体积混合,所得溶液的pH≤7
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高一阶段考一化学卷(解析版) 题型:选择题
NA为阿伏伽德罗常数的值,下列叙述错误的是( )
A.18 g H2O中含的 质子数为10 NA
质子数为10 NA
B.12 g  金刚石含有的电子数为4 NA
金刚石含有的电子数为4 NA
C.46 g NO2和N2O4混合气体中含有原子总数为3 NA
D.23 g Na 与足量 O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷(解析版) 题型:选择题
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒 容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)
容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)  2NH3(g)
2NH3(g)  kJ·mol
kJ·mol )
)
容器 | 甲 | 乙 | 丙 |
| 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
NH3的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
体系压强(pa) | p1 | p2 | p3 |
反应物转化率 | α1 | α2 | α3 |
请写出下列物理量的关系:
(1)浓度c1与c2_________________;2c2与c3________________
(2)能量a与b __________________;2b与c___________________
(3)压强p1与p2_________________;2p2与p3__________________
(4)转化率α1与α2________________;α2与α3___________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷(解析版) 题型:选择题
反应C(s)+H2O(g) CO(g)+H2(g)在一密闭容器中进行,下列说法或结论能够成立的是( )
CO(g)+H2(g)在一密闭容器中进行,下列说法或结论能够成立的是( )
A.当 v(CO)(正)=v(H2)(正)时,反应达平衡状态
B.其他条件不变,适当增加C(s)质量会使平衡正向移动
C.保持体积不变,充入少量He使体系压强增大,反应速率一定增大
D.其他条件不变仅将容器的体积缩小一半,再次平衡时H2O(g)的平衡浓度可能是原来的2.1倍
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷(解析版) 题型:选择题
在一个密闭容器中发生反应:2SO2(g)+O2(g) 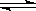 2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L、0.2 mol/L、0.2 mol/L,当反应达到反应限度时可能的数据是( )
2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L、0.2 mol/L、0.2 mol/L,当反应达到反应限度时可能的数据是( )
A.c(SO3)=0.4mol/L
B.c(SO2)=c(SO3)=0.15mol/L
C.c(O2)=0.35mol/L
D.c(SO2)+c(SO3)=0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应熵判据起决定作用 | B. | 该反应焓判据起决定作用 | ||
| C. | 该反应是熵减的反应 | D. | 该反应是分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com