
利用合成气(H2+CO)生产汽油、甲醇和氨等已经实现了工业化,合成气也可转化成醛、酸、酯等多种产物。下列表述正确的一组是 ( )。
①以合成气为原料的反应都是化合反应
②改变合成气中CO与H2的体积比,可以得到不同产物
③合成气的转化反应需在适当的温度和压强下通过催化完成
④从合成气出发生成液态烃或醇类有机物是实现“煤变油”的有效途径
⑤以合成气为原料的反应产物中不可能有烯烃或水
A.①②④ B.②③④
C.②④⑤ D.③④⑤
科目:高中化学 来源: 题型:
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1 mol
CuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是( )
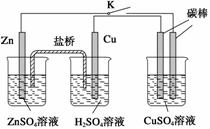
A.铜棒为正极,其电极反应式为2H++2e-—→H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13 g
D.导线中通过的电子的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
橡胶属于重要的工业原料。它是一种有机高分子化合物,具有良好的弹性,但强度较差。为了增强某些橡胶制品的强度,加工时往往需硫化处理,即将橡胶原料与硫黄在一定条件下反应。橡胶制品硫化程度越高,强度越大,弹性越差。下列橡胶制品中,加工时硫化程度较高的是 ( )。
A.橡皮筋 B.汽车外胎
C.普通气球 D.医用乳胶手套
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是 ( )。
A.石油中含有C6—C11的烷烃,可以通过石油的分馏得到汽油
B.含C18以上烷烃的重油经过催化裂化可以得到汽油
C.煤是有机化合物和无机化合物组成的复杂的混合物
D.煤的气化是为了使能源便于运输
查看答案和解析>>
科目:高中化学 来源: 题型:
随着现代工业的发展,能源问题已经越来越引起人们的重视。科 学家们预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适当的催化剂作用水解成葡萄糖,再将葡萄糖转化成乙醇,用作燃料。
学家们预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适当的催化剂作用水解成葡萄糖,再将葡萄糖转化成乙醇,用作燃料。
(1)写出将绿色植物的秸秆转化为乙醇的化学方程式
______________________ _____________________________。
_____________________________。
(2)已知:C2H5OH(l)+3O2(g)―→2CO2(g)+3H2O(l)
ΔH=-1 367 kJ·mol-1
CH4(g)+2O2(g)―→CO2(g)+2H2O(l)
ΔH=-890 kJ·mol-1
若某种植物的秸杆含纤维素约50%,由植物秸杆经过一系列转化得到乙醇原料的总利用率为80%,则用1 000 g秸杆为原料制得的乙醇燃料燃烧所产生的热量与 L甲烷完全燃烧产生的热量相当(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下的难溶电解质AmBn在水溶液中达到溶解平衡时。已知下表数据:
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH | ≥9.6 | ≥6.4 | 3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法中错误的是( )
A.向该溶液中加入少量铁粉不能观察到红色固体析出
B.该溶液中c(S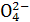 )∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
)∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
C.向该溶液中加入适量氯水,并调节pH到3~4后过滤,得到纯净的CuSO4溶液
D.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、A12O3、CaO、MgO等杂质)。用该烧渣制取药用辅料——红氧化铁的工艺流程如下:

(1)在“还原焙烧”中产生的有毒气体可能有 。
(2)“酸浸”时间一般不超过20 min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因是 (用离子方程式表示)。
(3)根据下表数据:
| 氢氧化物 | Al(OH)3 | Mg(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 3.10 | 8.54 | 2.01 | 7.11 |
| 完全沉淀的pH | 4.77 | 11.04 | 3.68 | 9.61 |
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于 ,检验Fe3+已经除尽的试剂是 ;当pH = 5时,溶液中c(Al3+)= mol·L– 1(已知常温下Ksp[Al(OH)3] = 2.0×10– 33)。
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,则A的操作是 。
(5)a g烧渣经过上述工艺可得红氧化铁b g。 药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于 (用含a、b的表达式表示)。
药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于 (用含a、b的表达式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
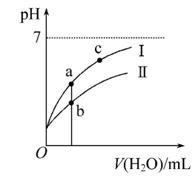
已知:25℃时某些弱酸的电离平衡常数如表所示。下面图像表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。下列说法中正确的是( )
| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.向NaClO溶液中通入少量二氧化碳的离子方程式为2ClO-+CO2+H2O====
2HClO+CO32-
C.图像中a、c两点处的溶液中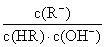 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)
D.图像中a点酸的总浓度大于b点酸的总浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com