
| A. | pH小于7的雨水被称为酸雨 | |
| B. | 推广使用燃煤脱硫技术,主要是为了防治SO2污染 | |
| C. | 为防止富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 | |
| D. | 明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒 |
分析 A.pH小于5.6的为酸雨;
B.推广使用燃煤脱硫技术,减少二氧化硫的排放;
C.生石灰或硅胶可吸收水,不具有还原性;
D.明矾中的铝离子水解生成胶体具有吸附性,不具有强氧化性.
解答 解:A.pH小于5.6的为酸雨,因雨水中溶解N、S的氧化物,酸性增强,故A错误;
B.推广使用燃煤脱硫技术,CaO与二氧化硫反应,从而减少二氧化硫的排放,则主要是为了防治SO2污染,故B正确;
C.生石灰或硅胶可吸收水,不具有还原性,只作干燥剂,不能抗氧化,故C错误;
D.明矾中的铝离子水解生成胶体具有吸附性,不具有强氧化性,则不能杀菌消毒,故D错误;
故选B.
点评 本题考查环境保护与物质的性质,为高频考点,把握物质的性质、发生的反应及化学与环境的关系是解本题关键,侧重分析与应用能力的考查,题目难度不大.


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:解答题
| 物质 | N2 | H2 | NH3 |
| 起始(mol) | 2 | 7 | 0 |
| 10s(mol) | 1.6 | ||
| 平衡(mol) | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项化合物 | A | B | C | D |
| Y | NH3 | Kl | MgO | H20 |
| W | HCl | KCl | C02 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
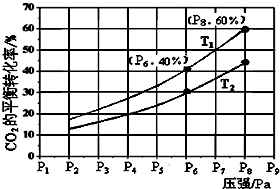
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
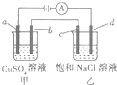 如图所示,a,b,c均为石墨电极,d为碳钢电极,通电电解一段时间,假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
如图所示,a,b,c均为石墨电极,d为碳钢电极,通电电解一段时间,假设在电解过程中产生的气体全部逸出,下列说法正确的是( )| A. | 甲、乙两烧杯中溶液的pH均保持不变 | |
| B. | 甲烧杯中b电极反应式为:Cu2++2e-═Cu | |
| C. | 当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 | |
| D. | 当b极增重3.2g时,d极产生的气体为0.56L(标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
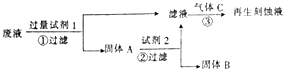 如图是处理蚀刻电路板废液(含有FeCl2、FeCl3、CuCl2)回收FeCl3溶液的方案,下列有关说法正确的是( )
如图是处理蚀刻电路板废液(含有FeCl2、FeCl3、CuCl2)回收FeCl3溶液的方案,下列有关说法正确的是( )| A. | 试剂1可以是铁也可以是铜 | |
| B. | 试剂2可以是盐酸也可以是硫酸 | |
| C. | 气体C为Cl2,不能用H2O2替换 | |
| D. | 步骤①②③中发生的反应均为氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com