
”¾ĢāÄæ”æFeÓėĻ”HNO3·“Ó¦Ź±£¬ČōĮ½ÕßĻūŗÄĪļÖŹµÄĮæÖ®±ČĪŖ4”Ć10£¬ĒŅÉś³É Fe(NO3)2£¬Ōņ·“Ó¦ÖŠÉś³ÉµÄ»¹Ō²śĪļæÉÄÜŹĒ£Ø £©
A.N2B.N2OC.NOD.NH4NO3
 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøŠ¹āŠŌøß·Ö×ÓŅ²³Ę”°¹āĆōŠŌøß·Ö×Ó”±£¬ŹĒŅ»ÖÖŌŚ²ŹµēÓ«¹āĘĮ¼°“ó¹ęÄ£¼Æ³ÉµēĀ·ÖĘŌģÖŠÓ¦ÓĆ½Ļ¹ćµÄŠĀŠĶøß·Ö×Ó²ÄĮĻ£¬Ęä½į¹¹¼ņŹ½ČēĻĀ

ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŌŚŅ»¶ØĢõ¼žĻĀ£¬øĆøß¾ŪĪļæÉ·¢ÉśµÄ·“Ó¦ÓŠ(ĢīŠ“±ąŗÅ)________”£
¢Ł¼Ó³É·“Ó¦””¢ŚŃõ»Æ·“Ó¦””¢ŪĻūČ„·“Ó¦””¢Üõ„»Æ·“Ó¦ ¢ŻĀ±“ś·“Ó¦
£Ø2£©øĆøß¾ŪĪļŌŚ“߻ƼĮµÄ×÷ÓĆĻĀĖ®½āµĆµ½Ļą¶Ō·Ö×ÓÖŹĮæ½ĻŠ”µÄ²śĪļA£¬AµÄĶ¬·ÖŅģ¹¹ĢåÓŠ¶ąÖÖ£¬ĘäÖŠŗ¬ÓŠ±½»·”¢ £¬ĒŅ±½»·ÉĻÓŠĮ½øö“¦ÓŚ¶ŌĪ»µÄČ”“ś»łµÄĪļÖŹµÄ½į¹¹¼ņŹ½æÉÄÜŹĒ__________________”£
£¬ĒŅ±½»·ÉĻÓŠĮ½øö“¦ÓŚ¶ŌĪ»µÄČ”“ś»łµÄĪļÖŹµÄ½į¹¹¼ņŹ½æÉÄÜŹĒ__________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫ĪļÖŹµÄĮæ¾łĪŖ0.1mol AlCl3”¢K2SO4ŗĶAl2£ØSO4£©3ČÜÓŚĖ®£¬ĻņĘäÖŠ¼ÓČėŅ»¶ØĮæµÄBa£ØOH£©2ČÜŅŗ£¬²āµĆČÜŅŗÓė³ĮµķÖŠ¾łŗ¬ÓŠĀĮŌŖĖŲ£¬ŌņÉś³ÉBaSO4µÄĪļÖŹµÄĮæ²»æÉÄÜĪŖ£Ø £©
A.0.2mol
B.0.25 mol
C.0.35 mol
D.0.45 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŗćČŻĆܱÕČŻĘ÷ÖŠæÉŅŌ×÷ĪŖ2NO2(g) ![]() 2NO(g)+O2(g)“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ( )
2NO(g)+O2(g)“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ( )
¢Łµ„Ī»Ź±¼äÄŚÉś³Én mol O2µÄĶ¬Ź±Éś³É2n mol NO2£»¢Śµ„Ī»Ź±¼äÄŚÉś³Én mol O2µÄĶ¬Ź±Éś³É2n mol NO£»¢Ū»ģŗĻĘųĢåµÄŃÕÉ«²»ŌŁøı䣻¢Ü»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁøıäµÄדĢ¬£»¢Ż»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»ŌŁøıäµÄדĢ¬£»¢Ž»ģŗĻĘųĢåÖŠNOÓėO2µÄĪļÖŹµÄĮæÖ®±Č±£³Öŗć¶Ø£»¢ß»ģŗĻĘųĢåÖŠNOÓėNO2µÄĪļÖŹµÄĮæÖ®±Č±£³Öŗć¶Ø
A. ¢Ł¢Ū¢Ż¢ß B. ¢Ś¢Ü¢Ż C. ¢Ł¢Ū¢Ü D. ¢Ł¢Ś¢Ū¢Ü¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗø½ÓøÖĢśŹ±³£ÓƵÄŗøŅ©ĪŖĀČ»Æļ§£¬Ęä×÷ÓĆŹĒĻū³żŗø½Ó“¦µÄĢśŠā£®·¢ÉśµÄ·“Ó¦ĢåĻµÖŠ¹²ÓŠĮłÖÖĪļÖŹ£ŗNH4Cl”¢FeCl3”¢N2”¢Fe2O3”¢FeŗĶX£®
£Ø1£©øł¾ŻĢāŅā£¬æÉÅŠ¶Ļ³öXŹĒ£ØŠ“»ÆѧŹ½£©£®
£Ø2£©Š“³ö²¢ÅäĘ½øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ£»
£Ø3£©·¢Éś»¹Ō·“Ó¦µÄĪļÖŹŹĒ £¬ ·“Ó¦ÖŠ2molµÄŃõ»Æ¼ĮÄÜ£ØĢī”°Ź§Č„”±»ņ”°µĆµ½”±£©molµē×Ó£®
£Ø4£©·“Ó¦ÖŠ±»Ńõ»Æ²śÉśĮĖ5.6L£Ø±ź×¼×“æö£©µÄĘųĢåŹ±£¬±»»¹ŌµÄĪļÖŹµÄÖŹĮæĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·“Ó¦ÖŠ£¬SO2×÷»¹Ō¼ĮµÄŹĒ£Ø £©
A.SO2+NaOH=NaHSO3
B.2Mg+3SO2=S+2MgSO3
C.SO2+2H2S=3S+2H2O
D.2KMnO4+5SO2+2H2O=2MnSO4+K2SO4+2H2SO4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹Ų»ÆѧÄÜÓėČČÄܵÄĖµ·ØÕżČ·µÄŹĒ
A. ĀĮČČ·“Ó¦ŹōÓŚĪüČČ·“Ó¦
B. Čōij·“Ó¦µÄ·“Ó¦ĪļµÄ×ÜÄÜĮæ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棬ŌņøĆ·“Ó¦ĪŖĪüČČ·“Ó¦
C. H2”śH+HµÄ±ä»ÆŠčŅŖĪüŹÕÄÜĮæ
D. ·²¾¼ÓČȶų·¢ÉśµÄ»Æѧ·“Ó¦¶¼ŹĒĪüČČ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶź³ÉĻĀĮŠÓŠ¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬²¢×¢Ć÷ÓŠ¹Ų·“Ó¦Ģõ¼ž£ŗ
£Ø1£©2-äå±ūĶéĻūČ„·“Ó¦·½³ĢŹ½________________________________£»
£Ø2£©1,3-¶”¶žĻ©µÄ¼Ó¾Ū·“Ó¦·½³ĢŹ½____________________________£»
£Ø3£©CH3CH2CHOÓėŠĀÖĘCu(OH)2·“Ó¦µÄ·½³ĢŹ½_________________£»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCOŹĒĻÖ“ś»Æ¹¤Éś²śµÄ»ł“”ŌĮĻ£¬ĻĀĮŠÓŠ¹ŲĪŹĢā¶¼ŗĶCOµÄŹ¹ÓĆÓŠ¹Ų”£
£Ø1£©ĄūÓĆCOÉś²śŅŅ“¼: 2CO(g)£«4H2(g)![]() CH3CH2OH(g)£«H2O(g)¦¤H1
CH3CH2OH(g)£«H2O(g)¦¤H1
ÓÖŅŃÖŖ£ŗH2O(l)£½H2O(g)¦¤H2 CO(g)£«H2O(g)![]() CO2(g)£«H2(g)¦¤H3
CO2(g)£«H2(g)¦¤H3
¹¤ŅµÉĻŅ²æÉĄūÓĆCO2£Øg£©ÓėH2£Øg£©ĪŖŌĮĻŗĻ³ÉŅŅ“¼£ŗ
2CO2£Øg£©£«6H2£Øg£©![]() CH3CH2OH£Øg£©£«3H2O£Øl£© ¦¤H
CH3CH2OH£Øg£©£«3H2O£Øl£© ¦¤H
Ōņ£ŗ¦¤HÓė¦¤H1”¢¦¤H2”¢¦¤H3Ö®¼äµÄ¹ŲĻµŹĒ£ŗ¦¤H£½_______________________”£
£Ø2£©Ņ»¶ØĢõ¼žĻĀ£¬H2”¢COŌŚĢå»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠ·¢ÉśČēĻĀ·“Ó¦£ŗ4H2£Øg£©+2CO£Øg£©![]() CH3OCH3£Øg£©+H2O£Øg£©”£ĻĀĮŠ“ėŹ©ÖŠÄܹ»Ķ¬Ź±Āś×ćŌö“ó·“Ó¦ĖŁĀŹŗĶĢįøßCO×Ŗ»ÆĀŹµÄŹĒ____£ØĢī×ÖÄø£©”£
CH3OCH3£Øg£©+H2O£Øg£©”£ĻĀĮŠ“ėŹ©ÖŠÄܹ»Ķ¬Ź±Āś×ćŌö“ó·“Ó¦ĖŁĀŹŗĶĢįøßCO×Ŗ»ÆĀŹµÄŹĒ____£ØĢī×ÖÄø£©”£
A£®Ź¹ÓĆøߊ§“߻ƼĮ B£®½µµĶ·“Ó¦ĪĀ¶Č
C. Ōö“óĢåĻµŃ¹Ēæ D£®²»¶Ļ½«CH3OCH3“Ó·“Ó¦»ģŗĻĪļÖŠ·ÖĄė³öĄ“
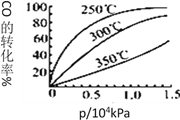
£Ø3£©²ÉÓĆCOÓėH2·“Ó¦ŗĻ³ÉŌŁÉśÄÜŌ“¼×“¼£¬·“Ó¦ČēĻĀ:CO£Øg£©+ 2H2£Øg£©![]() CH3OH£Øg£©”£ŌŚŅ»ČŻ»żæɱäµÄĆܱÕČŻĘ÷ÖŠ³äÓŠ10molCOŗĶ20mol H2£¬ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ӧɜ³É¼×“¼”£COµÄĘ½ŗā×Ŗ»ÆĀŹ£Ø¦Į£©ÓėĪĀ¶Č£ØT£©”¢Ń¹Ēæ£Øp£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£
CH3OH£Øg£©”£ŌŚŅ»ČŻ»żæɱäµÄĆܱÕČŻĘ÷ÖŠ³äÓŠ10molCOŗĶ20mol H2£¬ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ӧɜ³É¼×“¼”£COµÄĘ½ŗā×Ŗ»ÆĀŹ£Ø¦Į£©ÓėĪĀ¶Č£ØT£©”¢Ń¹Ēæ£Øp£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£

¢ŁŗĻ³É¼×“¼µÄ·“Ó¦ĪŖ_______£ØĢī ”°·ÅČČ”±»ņ”°ĪüČČ”±£©·“Ó¦”£
¢ŚA”¢B”¢CČżµćµÄĘ½ŗā³£ŹżKA”¢KB”¢KCµÄ“󊔹ŲĻµĪŖ_____________”£
¢Ū“ļµ½Ę½ŗāדĢ¬AŹ±£¬ČŻĘ÷µÄĢå»żĪŖ10L£¬ŌņŌŚĘ½ŗāדĢ¬BŹ±ČŻĘ÷µÄĢå»żĪŖ_________L”£
¢ÜCOµÄĘ½ŗā×Ŗ»ÆĀŹ£Ø¦Į£©ÓėĪĀ¶Č£ØT£©”¢Ń¹Ēæ£Øp£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬Źµ¼ŹÉś²śŹ±Ģõ¼žæŲÖĘŌŚ250”ę”¢1.3”Į104kPa×óÓŅ£¬Ń”Ōń“ĖŃ¹ĒæµÄĄķÓÉŹĒ________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com