
【题目】电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成。下列装置是用燃烧法确定有机物分子式常用的装置
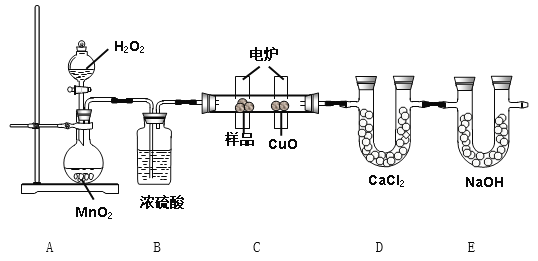
(1)A装置中MnO2的作用是________________;
(2)B装置中浓硫酸的作用是________________;
(3)燃烧管中CuO的作用是___________________;
(4)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取1.38 g样品,经充分反应后,D管质量增加1.62g,E管质量增加2.64g,则该样品的实验式(最简式)为_____________;
(5)要确定该物质的分子式,还要知道该物质的相对分子质量, 经测定其蒸气密度为2.054 g·L-1(已换算为标准状况下),则其分子式为________________;
(6)该物质的核磁共振氢谱如图所示,则其结构简式为__________________。

【答案】 催化作用(或催化剂) 干燥O2 使有机物充分氧化生成CO2和H2O C2H6O C2H6O CH3CH2OH
【解析】电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成。A装置是用双氧水制备氧气的,其中二氧化锰是作催化剂的。B装置用于干燥氧气。C装置中在电炉加热及氧化铜的作用下将有机物充分氧化为二氧化碳和水。D装置用于充分吸收水蒸气,通过该装置的增重测量生成物水的质量。E装置用于充分吸收产物二氧化碳,通过该装置增重测量二氧化碳的质量。
(1). A装置中MnO2的作用是 催化作用(或催化剂)
(2). B装置中浓硫酸的作用是干燥O2
(3). 燃烧管中CuO的作用是使有机物充分氧化生成CO2和H2O
(4). 样品只含C、H、O三种元素中的两种或三种, 1.38 g 样品,经充分反应后,D管质量增加1.62g是水的质量,求出n(H2O)=0.09mol,进一步求出n(H)=0.18mol,E管质量增加2.64g是二氧化碳的质量,求出n(C)=n(CO2)=0.06mol,根据质量守恒求出m(O)=1.38g-0.18g-0.06![]() 12g=0.48g,则n(O)=0.03mol,最后求出n(C):n(H):n(O)=2:6:1,所以该样品 的实验式(最简式)为C2H6O
12g=0.48g,则n(O)=0.03mol,最后求出n(C):n(H):n(O)=2:6:1,所以该样品 的实验式(最简式)为C2H6O
(5). 根据蒸气密度为2.054 g·L-1(已换算为标准状况下)可求出该有机物的相对分子质量为2.054![]() 22.4=46,与最简式的式量相同,所以其分子式为 C2H6O 。
22.4=46,与最简式的式量相同,所以其分子式为 C2H6O 。
(6).根据该有机物的核磁共振氢谱可知该有机物有3种氢原子,且个数比为1:2:3,所以该有机物的结构简式为 CH3CH2OH。


科目:高中化学 来源: 题型:
【题目】不能用胶体知识解释的是( )
A. 静电除尘
B. 一支钢笔用不同牌子的两种墨水,易堵塞
C. 氯化铁溶液加入氢氧化钠溶液出现红褐色沉淀
D. 河水和海水交界处形成三角洲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钌(Ru)是一种硬而脆呈浅灰色的多价稀有金属,性质很稳定,且耐腐蚀性很强。实验室用H2还原RuO2来制备金属钌的装置如图所示。下列说法不正确的是
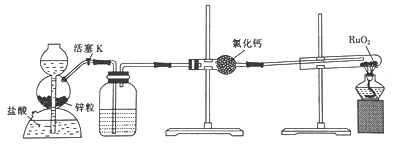
A. 加热试管前,应先收集气体并点燃,通过爆鸣声判断气体的纯度
B. 洗气瓶中盛装的可能是NaOH溶液,用于除去HCl
C. 结束反应时,先停止加热,再关闭活塞K
D. 启普发生器也可用于二氧化锰与浓盐酸反应制备氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了实现“将全球温度上升幅度控制在2℃以内”的目标,科学家正在研究温室气体CO2的转化和利用。
(1)海洋是地球上碳元素的最大“吸收池”
①溶于海水中的CO2主要以四种无机碳形式存在,分别为CO2、H2CO3、CO32-和_________(填离子符号)。
②在海洋中,可通过如图所示的途径来固碳。则发生光合作用时,CO2与H2O反应生成(CH2O)x和O2的化学方程式为__________________。

(2)有科学家提出可利用FeO来吸收CO2,已知:
C(s)+2H2O(g)![]() CO2(g)+2H2(g) △H=+113.4 kJ·mol-1
CO2(g)+2H2(g) △H=+113.4 kJ·mol-1
3FeO(s)+H2O(g)![]() Fe3O4(s)+H2(g) △H=+18.7 kJ·mol-1
Fe3O4(s)+H2(g) △H=+18.7 kJ·mol-1
则6FeO(s)+CO2(g)![]() 2Fe3O4(s)+C(s) △H=_____kJ·mol-1。
2Fe3O4(s)+C(s) △H=_____kJ·mol-1。
(3)以CO2为原料可制备甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),向一恒容密闭容器中充入1moCO2(g)和3molH2(g),测得CO2(g)和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g),向一恒容密闭容器中充入1moCO2(g)和3molH2(g),测得CO2(g)和CH3OH(g)的浓度随时间的变化如图所示。

①若A点的正反应速率用v正(CO2)来表示,A点的逆反应速率用v逆(CO2)来表示,则v正(CO2)_______(填“>”“ <”或“=”)v逆(CO2)。
②0~3min内,氢气的平均反应速率v(H2)_______________。
(4)在一定条件下,二氧化碳转化为甲烷:CO2(g)+4H2(g)![]() CH4(g)+2 H2O(g),△H。向一密闭容积正充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时测得c(CO2)= 0.2 mol·L-1,c(H2) =0.8 mol·L-1,c(H2O)=1.6mol·L-1。则该温度下上述反应的平衡常数K= ________。若200℃时该反应的平衡常数K=64.8,则该反应的△H_____(填“>’’或“<”)O。
CH4(g)+2 H2O(g),△H。向一密闭容积正充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时测得c(CO2)= 0.2 mol·L-1,c(H2) =0.8 mol·L-1,c(H2O)=1.6mol·L-1。则该温度下上述反应的平衡常数K= ________。若200℃时该反应的平衡常数K=64.8,则该反应的△H_____(填“>’’或“<”)O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种烃A对氢气的相对密度为36 ,已知该烃中碳氢两元素的质量比为5∶1,求:
(1)确定该烃的分子式____________。
(2)如果该烃的一氯取代物有4种,写出该烃的结构简式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据考证,商代炼铜,主要矿物原料是孔雀石,主要燃料是木炭,冶炼温度估计在1000℃左右,可能涉及的反应有:①Cu2(OH)2CO3 ![]() 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
②2CuO+C ![]() 2Cu+CO2↑
2Cu+CO2↑
③CuO+CO ![]() Cu+CO2
Cu+CO2
④CO2+C ![]() 2CO
2CO
(1)从四种基本反应类型看,①②④分别属于、、 .
(2)在上述反应中,属于氧化还原反应的是(填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将某强酸和某强碱溶液按1∶10的体积比混合后,溶液恰好呈中性,则混合前此强酸和强碱的pH和为( )
A.12
B.13
C.14
D.15
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com