
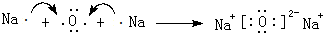 .
.分析 A、B、C、D、E为短周期元素,且原子序数依次增大,A、C能形成两种液态化合物A2C和A2C2,则A为H,C为O,形成的化合物为H2O和H2O2;A、D同主族,D的原子序数大于氧,所以D为Na;由原子序数可知,E处于第三周期,而E元素的周期序数与主族序数相等,则E为Al;五元素的质子数之和为40,则B的质子数为40-1-8-11-13=7,所以B为N元素,据此解答.
解答 解:A、B、C、D、E为短周期元素,且原子序数依次增大,A、C能形成两种液态化合物A2C和A2C2,则A为H,C为O,形成的化合物为H2O和H2O2;A、D同主族,D的原子序数大于氧,所以D为Na;由原子序数可知,E处于第三周期,而E元素的周期序数与主族序数相等,则E为Al;五元素的质子数之和为40,则B的质子数为40-1-8-11-13=7,所以B为N元素.
(1)由上述分析可知,B为N元素,C为O元素,
故答案为:N;O;
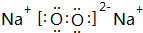
(2)Na2O2的电子式: ,
,
故答案为: ;
;
(3)用电子式表示D与C形成Na2O的过程: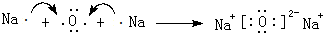 ,
,
故答案为: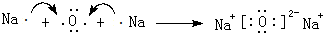 ;
;
(4)B的最高价氧化物对应的水化物为硝酸,其氢化物为氨气,二者反应方程式:HNO3+NH3=NH4NO3,
故答案为:HNO3+NH3=NH4NO3;
(5)D的最高价氧化物对应的水化物为NaOH,Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(6)A为NaH,能与水反应放氢气,则反应方程式为:NaH+H2O=NaOH+H2↑,
NaH+H2O=NaOH+H2↑
1mol 1mol 1mol
2NaOH+2Al+2H2O=2NaAlO2+3H2↑
1mol 1mol 1.5mol
n(H2)=1mol+1.5mol=2.5mol,
V(H2)=2.5mol×22.4L/mol=56L,
故答案为:NaH+H2O=NaOH+H2↑;56L;
(7)氢气、氧气制成新型的化学电源(KOH溶液作电解质溶液),正极发生还原反应,氧气在正极通入,负极发生氧化反应,氢气在负极失去电子,碱性条件下生成水,负极电极反应式为:H2-2e-+2OH-=2H2O,
故答案为:氧气;H2-2e-+2OH-=2H2O.
点评 本题考查元素化合物的推断、常用化学用语、化学计算等,A、C形成的化合物为推断突破口,需要学生具备扎实的基础和综合运用知识解决问题的能力,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 糖类是有甜的有机物 | |
| B. | 糖类物质又叫碳水化合物,因此所有的糖类均可用通式Cn(H2O)m来表示 | |
| C. | 糖类物质和碳水化合物没有实质的联系 | |
| D. | 糖类可以分为单糖和多糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青蒿素(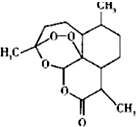 )可能具有氧化性 )可能具有氧化性 | |
| B. | “.煤改气”、“煤改电”等有利于减少雾霾天气 | |
| C. | 侯氏制碱法中,向饱和NaCI溶液中先通人NH3,再通人CO2 | |
| D. | 洁厕剂(含HCI )和漂白粉混合使用可使去污效果更好 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H>0、△S<0 | B. | △H<0、△S>0 | C. | △H>0、△S>0 | D. | △H<0、△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙中滴入盐酸 CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | Fe(OH)3 中滴入硫酸 OH-+H +═H2O | |
| C. | AgNO3中滴入NaCl溶液 Ag ++Cl-═AgCl↓ | |
| D. | CO2通入到足量NaOH溶液中CO2+2OH-═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的干馏,石油的裂化和裂解均属于化学变化 | |
| B. | 利用铝热反应可以冶炼Fe、Cr、Mn、W、Na等金属 | |
| C. | 甲烷和氯气制备一氯甲烷的原子利用率可达100% | |
| D. | SO2、NO2、CO2均是导致酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH<7.0的降水通常称为酸雨 | |
| B. | 燃煤时加入适量石灰石,可减少废气中SO2的量 | |
| C. | 新制氯水经光照一段时间pH增大 | |
| D. | 测定氯水的pH应用干燥的pH试纸,不能用蒸馏水润湿 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Al<Mg<F | B. | 热稳定性:HI>HBr>HCl>HF | ||
| C. | 酸性:H2SiO3<H3PO4<H2SO4<HClO4 | D. | 碱性:Al(OH)3>Mg(OH)2>NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含X与Y的化合物只有2种 | |
| B. | Y、W的氧化物均为酸性氧化物 | |
| C. | 最高价氧化物对应水化物的酸性:Y<W | |
| D. | X与Z形成的化合物中,各原子均满足8电子稳定结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com