
分析 (1)Qc=$\frac{{c}^{2}(NO)}{c({N}_{2})×c({O}_{2})}$=$\frac{(2.94×1{0}^{-4})^{2}}{2.50×1{0}^{-2}×4.0×1{0}^{-3}}$=8.6×10-4>K,所以初始状态不是化学平衡状态;
(2)因为Qc>K,所以平衡逆向移动.
解答 解:(1)Qc=$\frac{{c}^{2}(NO)}{c({N}_{2})×c({O}_{2})}$=$\frac{(2.94×1{0}^{-4})^{2}}{2.50×1{0}^{-2}×4.0×1{0}^{-3}}$=8.6×10-4>K,所以初始状态不是化学平衡状态;故答案为:否;
(2)因为Qc>K,所以平衡逆向移动,故答案为:逆向移动.
点评 本题考查了平衡常数含义和表达式的计算应用,掌握基础是关键,题目较简单.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3CHO→C2H5OH | B. | C2H5Cl→CH2=CH2 | ||
| C. | C3H7Br→C3H7OH | D. | CH3COOH→CH3COOC2H5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阳极发生氧化反应,其电极反应式主要是:Ni-2e-=Ni2+ | |
| B. | 电解过程中,阳极质量的减少与阴极质量的增加不相等 | |
| C. | 电解后,溶液中存在的金属阳离子只有Fe2+、Ni2+和Zn2+ | |
| D. | 电解后,电解槽底部的阳极泥中只有Pt |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰→水若自发进行,△H<T△S | B. | 水→冰若自发进行,△H<0 | ||
| C. | 冰?水的平衡状态△H=T△S | D. | 水?冰的平衡状态,△H=0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸与KOH溶液 | B. | 氢氧化铜与盐酸 | ||
| C. | NaHSO4溶液与氨水 | D. | 硝酸与Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
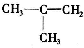 、CH3CH=CHCH3和CH3CH2CH=CH2.
、CH3CH=CHCH3和CH3CH2CH=CH2. ,其产物的名称是聚乙烯;乙烯对水果具有催熟功能.
,其产物的名称是聚乙烯;乙烯对水果具有催熟功能.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑥ | B. | ①② | C. | ③⑤ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 粒子 | A+ | B2- | C | D | E | F |
| 组成特点 | 单核离子 | 化合物, 双核分子 | 单质, 双核分子 | 化合物, 三核分子 | 化合物, 四核分子 | |
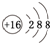 .
.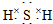 ;F的水溶液常用于消毒剂,F的化学式是H2O2.
;F的水溶液常用于消毒剂,F的化学式是H2O2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com