
【题目】下列实验装置正确的是( )
A.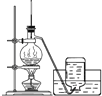 实验室制乙烯B.
实验室制乙烯B.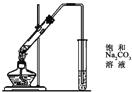 酯化反应
酯化反应
C.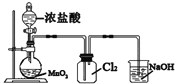 实验室制取Cl2D.
实验室制取Cl2D.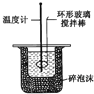 中和热的测定
中和热的测定
【答案】D
【解析】
A. 实验室制取乙烯需要170℃,温度计测量温度为溶液温度;
B. 酯化反应中导气管不能伸入饱和碳酸钠溶液中;
C. 制取氯气时,尾气处理应该防止倒吸现象;
D. 中和热测定中,温度计测量混合溶液温度,用环形玻璃棒搅拌溶液。
A. 实验室制取乙烯需要170℃,温度计要测量溶液温度,所以温度计应该插入溶液中,A错误;
B. 酯化反应中导气管不能伸入饱和碳酸钠溶液中,否则会产生倒吸现象,B错误;
C. 制取氯气时,尾气处理应该要防止倒吸,尾气处理装置中应该有倒置的漏斗,C错误;
D. 中和热测定中,温度计测量混合溶液温度,用环形玻璃棒搅拌溶液,使溶液温度混合均匀,符合实验条件,D正确;
故合理选项是D。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作与预期实验目的或所得实验结论一致的是
选项 | 实验操作和现象 | 预期实验目的或结论 |
A | 某溶液中滴加 | 说明该溶液中有 |
B | 向含有AgCl和 | 可说明Ksp(AgBr)<Ksp(AgCl) |
C | 分别向2支盛有4mL浓度为0.01 | 探究浓度对反应速率的影响 |
D | 在相同条件下,向一支试管中加入2mL5%的 | 探究催化剂对 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ。且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为( )
A.920 kJB.557 kJC.188 kJD.436 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到目的的是( )
选项 | 目的 | 实验 |
A | 检验某品牌食盐是否为加碘盐 | 将样品溶解后滴加淀粉溶液 |
B | 检验补铁剂硫酸亚铁片是否部分氧化 | 取样品溶解于水,滴加铁氰化钾溶液 |
C | 鉴别葡萄糖溶液和蔗糖溶液 | 分别取样,滴加银氨溶液,水浴加热 |
D | 证明 | 将 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍在工业上应用广泛,请回答下列问题。
(1) Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是____(用元素符号表示)。
(2) 过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=____。与CO互为等电子体的阴离子是____(只写一种),CO分子内σ键与π键个数之比为____。1mol Ni(CO)n中含σ键为____ mol。
(3) 甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醛分子内C原子的杂化方式为____,甲醇分子内的O—C—H键角____(填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学家在实验室中将CoCl2·6H2O溶解在煮沸的NH4Cl溶液后,趁热倒入盛有少量活性炭的锥形瓶中,冷却后依次加入浓氨水和H2O2,经过一系列的反应,最终制得了一种橙黄色晶体X,为确定其组成,进行如下实验:
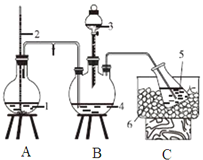
实验一、氨的测定:精确称取w gX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mLc1 mol/L的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mLNaOH溶液。
实验二、氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)
回答下列问题:
(1)图中2是一个长玻璃管,其作用原理是______。
(2)样品中氨的质量分数表达式为______。
(3)测定氨前应进行的操作是______。
(4)测定氯的过程中,使用棕色滴定管的原因是______,滴定终点的现象是______,若溶液中c(Ag+)=2.0×10-5mol/L,c(CrO42-)为______mol/L。(已知:Ksp(Ag2CrO4=1.12×10-12)
(5)经测定,样品X中钴、氨和氯的物质的量之比为1:6:3,钴的化合价为______,X的制备过程中温度不能过高的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是![]()
A.动物体内葡萄糖被氧化成![]() 是热能转变成化学能的过程
是热能转变成化学能的过程
B.![]() 与
与![]() 反应生成
反应生成![]() 沉淀时放出的热叫做中和热
沉淀时放出的热叫做中和热
C.热化学方程式中的化学计量数只表示物质的量,可以是分数
D.![]() 与
与![]() 反应放出的热就是
反应放出的热就是![]() 的燃烧热
的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:
2CH3COOH。现以A为主要原料合成化合物E,其合成路线如图1所示。回答下列问题:

(1)写出下列物质的官能团名称:B:____________________;D:____________________。
(2)反应④的化学方程式为________________________________________________,反应类型:________。
(3)某学习小组设计物质B催化氧化的实验装置如下,根据图2装置回答问题。

①装置甲锥形瓶中盛放的固体药品可能为________(填字母)。
A.Na2O2 B.KClC.Na2CO3 D.MnO2
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_______________________________。
③物质B的催化氧化产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水![]() 是一种重要的化工原料。某课外探究小组尝试制取无水
是一种重要的化工原料。某课外探究小组尝试制取无水![]() ,查阅资料获得下列信息:无水
,查阅资料获得下列信息:无水![]() 在
在![]() 升华,极易潮解,遇到水蒸气会产生白色烟雾。
升华,极易潮解,遇到水蒸气会产生白色烟雾。
探究一无水![]() 的实验室制备
的实验室制备
利用如图装置,用干燥、纯净的氯气在加热条件下与铝粉![]() 已除去氧化膜
已除去氧化膜![]() 反应制取无水AlCl3。供选择的药品:①铝粉②浓硫酸③稀盐酸④饱和食盐水⑤二氧化锰粉末⑥无水氯化钙⑦稀硫酸⑧浓盐酸⑨氢氧化钠溶液
反应制取无水AlCl3。供选择的药品:①铝粉②浓硫酸③稀盐酸④饱和食盐水⑤二氧化锰粉末⑥无水氯化钙⑦稀硫酸⑧浓盐酸⑨氢氧化钠溶液
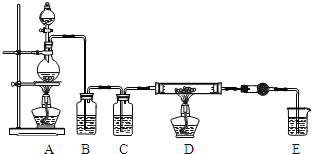
(1)写出装置A烧瓶中发生的反应方程式 ______ 。
(2)实验开始前,先检查装置气密性,然后装入药品,接下来的步骤依次是 ______ ![]() 填序号
填序号![]() 。
。
![]() 加热D中硬质玻璃管
加热D中硬质玻璃管
![]() 往A烧瓶中加入液体
往A烧瓶中加入液体
![]() 点燃A中的酒精灯
点燃A中的酒精灯
(3)上述供选药品中本实验无需用到的是 ______ ![]() 填数字序号
填数字序号![]() 。
。
(4)写出无水![]() 与水蒸气反应的化学方程式 ______ 。
与水蒸气反应的化学方程式 ______ 。
探究二无水![]() 的含量测定及结果分析
的含量测定及结果分析
取D中反应后所得固体![]() ,与足量氢氧化钠溶液反应,测定生成气体的体积
,与足量氢氧化钠溶液反应,测定生成气体的体积![]() 体积均换算成标准状况
体积均换算成标准状况![]() ,重复测定三次,数据如下:
,重复测定三次,数据如下:
第一次实验 | 第二次实验 | 第三次实验 | |
D中固体用量 |
|
|
|
氢气的体积 |
|
|
|
(5)根据表中数据,计算所得固体中无水![]() 的质量分数 ______ 。
的质量分数 ______ 。
(6)有同学认为测得的无水![]() 的质量分数偏低,你认为可能的原因有 ______ 。
的质量分数偏低,你认为可能的原因有 ______ 。
探究三离子浓度对氯气制备的影响
二氧化锰粉末和浓盐酸的反应随着盐酸的浓度降低,反应停止不再产生氯气。探究小组对盐酸浓度降低影响氯气生成的原因进行如下探究:
(7)提出假设假设1:![]() 浓度降低影响氯气的生成
浓度降低影响氯气的生成
假设2: ______ 。
(8)设计方案进行实验。限选试剂:浓![]() 、NaCl固体、
、NaCl固体、![]() 固体、稀盐酸。
固体、稀盐酸。
步骤 | 实验操作 | 预测现象和结论 |
| 往不再产生氯气的装置中,加入 ______ ,继续加热 | 若有黄绿色气体生成,则假设1成立 |
| ______ | 若有黄绿色气体生成,则假设2成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com