

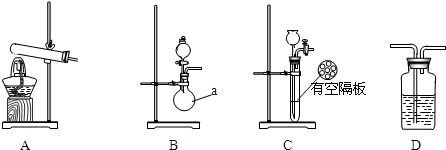
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为① (NH4)2SO4+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaSO4. |
| 乙小组 | ②B | 浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用: ③氢氧化钠溶于氨水后放热,增加氢氧根浓度,使NH3+H2O?NH3•H2O?NH4++OH-向逆反应方向移动,加快氨气逸出. |
分析 (1)给A装置连接一导管,将导管插入水中,形成密闭体系,加热试管,根据现象判断;
(2)氢氧化钙和硫酸铵反应生成氨气、硫酸钙和水;利用氢氧化钠固体溶解放热促进氨水溶液中平衡向放氨气的方向进行;
(3)根据氧化铜中氧元素的质量等于生成的水中氧元素的质量,根据氮气的体积计算出氮气的物质的量,从而求出氮原子的个数;
(4)利用碱石灰吸收水称量质量计算氢元素.
解答 解:(1)给A装置连接一导管,将导管插入水中,形成密闭体系,加热试管,导管口有气泡产生;停止加热,由于试管内压强减小,导管内有水回流并形成一段稳定的水柱;
故答案为:连接导管,将导管插入水中;加热试管,导管口有气泡产生;停止加热,导管内有水回流并形成一段稳定的水柱;
(2)甲组氢氧化钙与硫酸铵反应生成硫酸钙、氨气和水,反应的化学方程式为(NH4)2SO4+Ca(OH)2═2NH3↑+2H2O+CaSO4,
乙组中,氢氧化钠溶于氨水后放热、增加氢氧根浓度,使NH3+H2?NH3•H2?NH4++OH-向逆方向移动,加快氨气逸出,实验装置为B;
故答案为:①(NH4)2SO4+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaSO4;③氢氧化钠溶于氨水后放热,增加氢氧根浓度,使NH3+H2O?NH3•H2O?NH4++OH-向逆反应方向移动,加快氨气逸出;②B;
(3)反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g,则氧化铜中氧元素的质量为m1-m2,生成的水中氧元素的质量等于氧化铜氧元素的质量,则生成的水中氧原子的物质的量为$\frac{{m}_{1}-{m}_{2}}{16}$mol;水中氢原子物质的量是氧原子物质的量的两倍,因此氢原子物质的量为$\frac{{m}_{1}-{m}_{2}}{16}$×2mol,生成的氮气在标准状况下的体积V1L,则氮气中氮原子的物质的量为$\frac{{V}_{1}×2}{22.4}$mol;
因此氮氢原子个数比为$\frac{{V}_{1}×2}{22.4}$:$\frac{{m}_{1}-{m}_{2}}{16}$×2=5V1:7(m1-m2);
故答案为:5V1:7(m1-m2);
(4)因此在洗气瓶D前的位置应增加了一个装有碱石灰(氢氧化钠、氧化钙等)的实验仪器吸收水,减小误差,
故答案为:碱石灰(氢氧化钠、氧化钙等).
点评 本题是一道综合性很强的实验探究题,要求学生具有分析和解决问题的能力,主要是物质探究物质组成和方法的应用,掌握基础和基本操作是关键,难度中等.


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:选择题
| A. | X2Y3 | B. | X3Y2 | C. | Y2X3 | D. | Y3X2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol/L H2SO 4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn2C | B. | Al4C3 | C. | Mg2C3 | D. | Li2C2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.45 mol/L | B. | 0.6 mol/L | C. | 0.9 mol/L | D. | 1.2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去液溴中少量的氯水,可向其中加少量KI | |
| B. | 氯水和氯气均能使湿润的有色布条褪色,都是HClO作用的结果 | |
| C. | 某白色晶体与NaOH浓溶液混合,有能使湿润红色石蕊试纸变蓝的气体产生,则该晶体一定是NH4Cl | |
| D. | 某溶液能使淀粉碘化钾试纸变蓝,则溶液中一定含有Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com