
| m |
| M |
| V |
| Vm |
| N |
| NA |
| 1g |
| 2g/mol |
| 44.8L |
| 22.4L/mol |
| 6.02×1023 |
| 6.02×1023mol-1 |


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
131 53 |
131 53 |
| A、核外电子数为78 | ||
B、与
| ||
| C、中子数为131 | ||
D、与
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl- CO Na+、 |
| B、Na Cl- S2- |
| C、Fe3+ SO42- NO3- |
| D、Fe2+ O2 H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
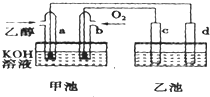 如图甲池和乙池中的四个电极都是惰性材料,溶液体积均为200mL,请根据图示回答下列问题
如图甲池和乙池中的四个电极都是惰性材料,溶液体积均为200mL,请根据图示回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从溴水中提取溴可用酒精作为萃取剂 |
| B、检验碘化钾溶液可用淀粉 |
| C、分离碘和食盐可用加热的方法 |
| D、用加热的方法除去铜中混有的氧化铜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com