
工业上常用氯氧化法处理含氰(CN-)废水,一定条件下,氯气和CN-反应生成无毒气体。下列说法不正确的是
A.CN-中碳元素的化合价为+2
B.该反应的产物之一是无毒的N2
C.当1 mol CN-参与反应时,转移3 mol e-
D.处理含0.1 mol CN-的废水,理论上需要消耗标准状况下Cl2的体积为5.6 L
科目:高中化学 来源: 题型:
根据离子方程式:( )+XO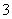 +6H+===3X2+3H2O判断,下列说法正确的是( )
+6H+===3X2+3H2O判断,下列说法正确的是( )
A.X2的电子式为X⋮⋮X
B.X位于元素周期表中第ⅤA族
C.X元素原子的最外层有7个电子
D.X可能位于元素周期表中第二周期
查看答案和解析>>
科目:高中化学 来源: 题型:
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.
已知:SO2(g)+1/2O2(g)⇌SO3(g)△H=﹣98kJ•mol﹣1.
(1)某温度下该反应的平衡常数K=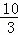 ,若在此温度下,向100L的恒容密闭容器中,充入3.0mol SO2(g)、16.0mol O2(g)和3.0mol SO3(g),则反应开始时v(正) v(逆)(填“<”、“>”或“=”).
,若在此温度下,向100L的恒容密闭容器中,充入3.0mol SO2(g)、16.0mol O2(g)和3.0mol SO3(g),则反应开始时v(正) v(逆)(填“<”、“>”或“=”).
(2)一定温度下,向一带活塞的体积为2L的密闭容器中充入2.0mol SO2和1.0mol O2,达到平衡后体积变为1.6L,则SO2的平衡转化率为 .
(3)在(2)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是 (填字母).
A.保持温度和容器体积不变,充入1.0mol O2
B.保持温度和容器内压强不变,充入1.0mol SO3
C.降低温度
D.移动活塞压缩气体
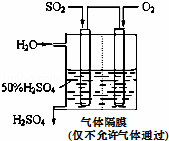
(4)若以如图所示装置,用电化学原理生产硫酸,写出通入O2电极的电极反应式为 .
(5)为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
N2(g)+3H2(g) 2NH3(g) △H<0。当反应达到平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0。当反应达到平衡时,下列措施能提高N2转化率的是
① 降温 ② 恒压通入惰性气体 ③ 增加N2的浓度 ④ 加压
A.①④ B.①② C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物PAS-Na是一种治疗肺结核药物的有效成分,有机物G是一种食用香料,以甲苯为原料合成这两种物质的路线如下:
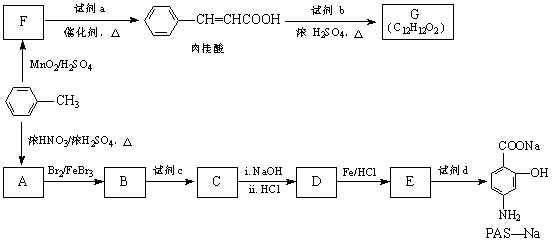

回答下列问题:
(1)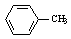 生成A的反应类型是 。
生成A的反应类型是 。
(2)F中含氧官能团的名称是 ;试剂a的结构简式为 。
(3)写出由A生成B的化学方程式: 。
(4)质谱图显示试剂b的相对分子质量为58,分子中不含甲基,且为链状结构,写出肉桂酸与试剂b生成G的化学方程式: 。
(5)当试剂d过量时,可以选用的试剂d是 (填字母序号)。
a.NaHCO3 b.NaOH c.Na2CO3
(6)写出C与NaOH反应的化学方程式 。
(7)肉桂酸有多种同分异构体,符合下列条件的有 种。
a.苯环上有三个取代基;
b.能发生银镜反应,且1 mol该有机物最多生成4 mol Ag。
由上述符合条件的同分异构体中,写出苯环上有两种不同化学环境氢原子的有机物的结构简式(任写一种即可) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.化学反应中的能量变化,只表现为热量的变化
B.煤和石油属于可再生能源
C.汽车排出大量尾气中含有CO会污染大气
D.要使燃料燃烧只需要大量的氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
A.用物质A表示的反应平均速率为0.3 mol·L-1·s-1
B.用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
C.2 s时物质A的转化率为70%
D.2 s时物质B的浓度为0.7 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关反应原理及其应用,不正确的是( )
A.苯与浓硝酸反应;制备TNT炸药
B.葡萄糖能与新制Cu(OH)2悬浊液反应;尿糖检测
C.醋酸能与CaCO3、Mg(OH)2等反应;用食醋除去暖瓶中的水垢
D.乙烯能与水反应生成乙醇;制取工业酒精
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com