
分析 (1)①根据反应4NO2+O2+2H2O=4HNO3分析原混合气体中NO2和O2的体积比;根据n=$\frac{V}{{V}_{m}}$、c=$\frac{n}{V}$计算;
②根据反应3NO2+H2O=2HNO3+NO可知剩余的气体不可能为NO,利用差量法计算出反应消耗的二氧化氮、氧气体积,然后得出氧气总体积,再计算出原混合气体中NO2和O2的体积比;
(2)实际参加反应的NO2比NH3少2mL,由6NO2+8NH3=7N2+12H2O可知,参加反应的NO2、NH3的体积分别为6mL、8mL,故剩余气体为20mL-6mL-8mL=6mL,剩余气体可能为NO2,可能为NH3,据此讨论计算.
解答 解:(1)①若一段时间内水上升且充满试管,说明二氧化氮和氧气恰好反应,根据方程式4NO2+O2+2H2O=4HNO3可知原混合气体中NO2和O2的体积比为4:1;
设试管容积为VL,则试管中气体的物质的量为:$\frac{VL}{22.4L/mol}$=$\frac{V}{22.4}$mol,根据反应4NO2+O2+2H2O=4HNO3可知生成硝酸的物质的量为:$\frac{V}{22.4}$mol×$\frac{4}{5}$=$\frac{V}{28}$mol,则所得溶液中硝酸的浓度为:$\frac{\frac{V}{28}mol}{VL}$≈0.036mo/L,
故答案为:4:1;0.036mo/L;
②若一段时间后上升的水只升到试管容积的一半,根据反应3NO2+H2O=2HNO3+NO可知,若剩余的NO,则原混合物中含有的二氧化氮体积为原先总体积的$\frac{1}{2}$×3=$\frac{3}{2}$>1,剩余剩余的气体为O2;设试管容积为VL,则反应4NO2+O2+2H2O=4HNO3中消耗的二氧化氮的体积为:$\frac{1}{2}$VL×$\frac{4}{5}$=$\frac{2}{5}$VL,原混合气体中含有氧气的体积为$\frac{3}{5}$L,原混合气体中,NO2和O2的体积比是:$\frac{2}{5}$VL:$\frac{3}{5}$L=2:3,
故答案为:O2;2:3;
(2)实际参加反应的NO2比NH3少2mL,由6NO2+8NH3=7N2+12H2O可知,参加反应的NO2、NH3的体积分别为6mL、8mL,故剩余气体为20mL-6mL-8mL=6mL,
若剩余气体为NO2,则V(NO2)=6mL+6mL=12mL,物质的量之比等于体积之比,故n(NO2):n(NH3)=V(NO2):v(NH3)=12mL:8mL=3:2,
若剩余气体为NH3,则v(NH3)=8mL+6mL=14mL,物质的量之比等于体积之比,故n(NO2):n(NH3)=V(NO2):v(NH3)=6mL:14mL=3:7,
故答案为:BD.
点评 本题考查了有关讨论的计算、混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握讨论法在化学计算中的应用方法,试题培养了学生的化学计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 铁的金属活泼性强,故不能用钢瓶来盛放液氯 | |
| B. | Na2O2与CO2能反应产生氧气,用作呼吸面具和潜水艇供氧剂 | |
| C. | NaHCO3受热能分解产生CO2气体,在食品工业中可作为焙制糕点的膨松剂 | |
| D. | 常温下浓硫酸能使铝发生钝化,常温下可用铝制容器贮藏贮运浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种物质所含原子个数之比为4:3 | |
| B. | 两种物质与水充分反应,生成的氢氧化钠质量之比为2:1 | |
| C. | 两种物质与足量的CO2反应,消耗气体的质量比为1:1 | |
| D. | 两种物质中阳离子的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ③④⑤⑥ | C. | ②③④⑤ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌 | B. | 铁 | C. | 镁 | D. | 铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:SO2>I->Fe2+,用如图所示装置进行实验(加热和夹持装置已略,气密性已检验).
某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:SO2>I->Fe2+,用如图所示装置进行实验(加热和夹持装置已略,气密性已检验).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
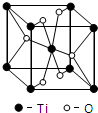 第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.
第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V L该气体的质量(以g为单位) | B. | 1 L该气体的质量(以g为单位) | ||
| C. | 1 mol该气体的体积(以L为单位) | D. | 1 L该气体的物质的量(以mol为单位) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 57.6% | B. | 42.4% | C. | 53.6% | D. | 46.4% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com