
 2013年12月2日,我国“嫦娥三号”探测器由长征三号运载火箭发射,首次实现月球软着陆和月面巡视勘察.“玉兔”月球车底盘和车轮由铝合金材料制成.看见玉兔车金灿灿的车身后,小聪同学想到家里新换的水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请你一同参加.
2013年12月2日,我国“嫦娥三号”探测器由长征三号运载火箭发射,首次实现月球软着陆和月面巡视勘察.“玉兔”月球车底盘和车轮由铝合金材料制成.看见玉兔车金灿灿的车身后,小聪同学想到家里新换的水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请你一同参加.| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 | 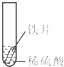 | 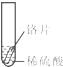 | 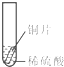 |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 铜表面无气泡,溶液不变色 |
分析 (1)金属活动性顺序表中金属排列顺序是:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au;
(2)还有一种猜想是Cr的金属性活动性介于Fe和Cu之间;
(3)在金属活动性顺序表中Cu位于H之后,Cu和弱氧化性酸不反应;
(4)金属的金属性越强,其单质越容易置换出酸中的氢元素;
(5)Cr的活泼性大于Fe,所以Cr能置换出亚铁盐中的铁.
解答 解:(1)金属活动性顺序表中金属排列顺序是:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au,故答案为:Hg;
(2)还有一种猜想是Cr的金属性活动性介于Fe和Cu之间,即金属活动性Fe>Cr>Cu,故答案为:Fe>Cr>Cu;
(3)试管1说明Fe和稀硫酸发生置换反应生成氢气但反应速率较慢,试管2说明Cr和稀硫酸发生置换反应且反应速率较试管1块,金属的金属性越强,其单质越容易置换出酸中的氢元素,所以金属性Cr>Fe,在金属活动性顺序表中Cu位于H之后,所以Cu和稀硫酸不反应,则试管3看到的现象是铜表面无气泡,溶液不变色,
故答案为:铜表面无气泡,溶液不变色;
(4)根据(3)知金属活动性顺序是Cr>Fe>Cu,所以猜想1正确,故答案为:1;
(5)根据(3)知金属活动性顺序是Cr>Fe>Cu,所以Cr能和硫酸亚铁发生置换反应生成Fe,反应方程式为Cr+FeSO4=CrSO4+Fe,故答案为:能;Cr+FeSO4=CrSO4+Fe.
点评 本题以金属的活动性强弱为载体考查性质实验方案设计,明确实验原理是解本题关键,采用对比方法确定金属性强弱,同时考查学生实验设计、实验操作、观察及总结归纳能力,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:1 | B. | 3:2:3 | C. | 2:5:2 | D. | 1:2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
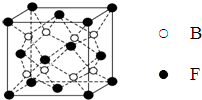 已知A、B、C、D、E、F、G、H、I为元素周期表中原子序数依次增大的前四周期元素,A原子的最外层中p轨道上的电子数等于前一电子层电子总数;A、B、C、D;E、F与G分别位于同一周期.C原子L层上有2对成电子,D、E、F的核外电子排布相同的简单离子可形成一种E3FD6型离子晶体X,EG、HC为电子数相同的离子晶体.I原子M层为全充满状态,且核外的未成对电子只有一个.请根据以上情况,回答下列问题:(答题时,用对应的元素符号表示)
已知A、B、C、D、E、F、G、H、I为元素周期表中原子序数依次增大的前四周期元素,A原子的最外层中p轨道上的电子数等于前一电子层电子总数;A、B、C、D;E、F与G分别位于同一周期.C原子L层上有2对成电子,D、E、F的核外电子排布相同的简单离子可形成一种E3FD6型离子晶体X,EG、HC为电子数相同的离子晶体.I原子M层为全充满状态,且核外的未成对电子只有一个.请根据以上情况,回答下列问题:(答题时,用对应的元素符号表示)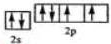 ;H离子电子排布式1s22s22p63s23p6;I位于周期表ds区;D在周期表中的位置第二周期ⅤⅡA族
;H离子电子排布式1s22s22p63s23p6;I位于周期表ds区;D在周期表中的位置第二周期ⅤⅡA族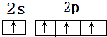 ,不符合能量最低原理原理.
,不符合能量最低原理原理.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
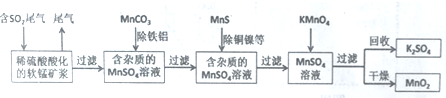
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素 | A | B | R | D |
| 相关信息 | 基态原子核外电子占据3个能级且最高能级上有3个电子 | B的单质是最常见半导体材料 | 位于第四周期ⅠB族 | 是非金属元素,其形成的某种单质是电的良导体,有的分子形状似足球 |
| 键能(kJ/mol) | 熔点(K) | 沸点(K) | |
| BO2 | B-O:452 | 1923 | 2503 |
| DO2 | D=O:615,D-O:348 | 216 | 195 |
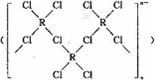 ,研究表明•
,研究表明•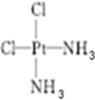 ( AH3配体作为一个整体写).
( AH3配体作为一个整体写).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 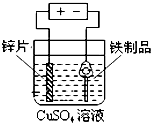 铁制品表面镀锌 | B. | 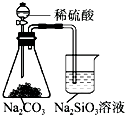 验证碳酸酸性强于硅酸 | ||
| C. | 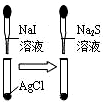 说明溶解性AgCl<AgI<Ag2S | D. |  浸在冷水中的玻璃球颜色较深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 16种 | C. | 32种 | D. | 64种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com