
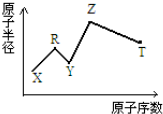
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 简单的气态氢化物的沸点和稳定性排序均为:Y>T | |
| C. | 最高价氧化物对应的水化物的酸性:T<R | |
| D. | 由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性 |
分析 R原子最外层电子数是电子层数的2倍,可能为C或S,由于图示原子半径和原子序数关系可知R应为C;Y与Z能形成Z2Y、Z2Y2型离子化合物,应为Na2O、Na2O2,则Y为O,Z为Na;Z与T形成的Z2T化合物能破坏水的电离平衡,T应为S,Na2S水解呈碱性,可促进水的电离;X的原子半径最小,原子序数最小,应为H元素,结合对应单质、化合物的性质以及题目要求解答该题.
解答 解:R原子最外层电子数是电子层数的2倍,可能为C或S,由于图示原子半径和原子序数关系可知R应为C;Y与Z能形成Z2Y、Z2Y2型离子化合物,应为Na2O、Na2O2,则Y为O,Z为Na;Z与T形成的Z2T化合物能破坏水的电离平衡,T应为S,Na2S水解呈碱性,可促进水的电离;X的原子半径最小,原子序数最小,应为H元素.
A.原子半径O>Na,离子半径O2->Na+,故A错误;
B.Y、T的简单氢化物分别为H2O、H2S,水分子之间存在氢键,沸点最高,故沸点H2O>H2S,非金属性越强氢化物越稳定,所以氢化物的稳定性H2O>H2S,故B正确;
C.非金属性S>C,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故C错误;
D.由H、C、O、Na四种元素组成的化合物不仅仅为NaHCO3,可能为有机盐且含有羧基,溶液不一定为碱性,可能为酸性,故D错误.
故选B.
点评 本题考查结构性质位置关系应用,侧重于学生的分析能力的考查,推断元素是解题的关键,D为易错点,学生容易忽略有机物,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ns电子的能量可能低于(n-1)p电子的能量 | |
| B. | 6C的电子排布式1s22s22px2反了洪特规则 | |
| C. | 电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理 | |
| D. | 电子排布式(22Ti)1s22s22p63s23p10违反了泡利原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
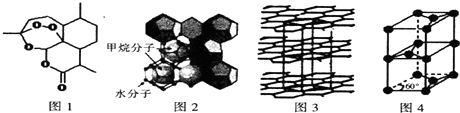
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
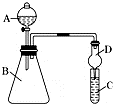 某同学欲利用图装置验证同主族元素性质递变规律.
某同学欲利用图装置验证同主族元素性质递变规律.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
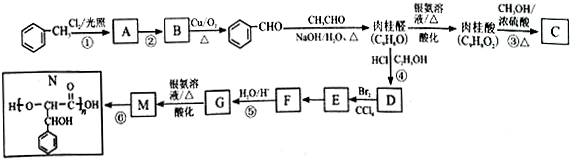
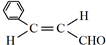 .
. .
.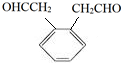 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15L | B. | 20L | C. | 23L | D. | 24L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性高锰酸钾溶液、溴水 | B. | 酸性高锰酸钾溶液、碳酸钠溶液 | ||
| C. | 酸性高锰酸钾溶液、氢氧化钠溶液 | D. | 酸性高锰酸钾溶液、氯化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
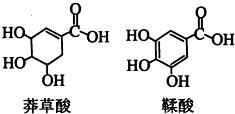 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )| A. | 两种酸都能与溴水反应且反应的原理相同 | |
| B. | 两种酸遇三氯化铁溶液都显色 | |
| C. | 鞣酸分子与莽草酸分子相比多了两个碳碳双键 | |
| D. | 等物质的量的两种酸与足量金属钠反应产生氢气的量相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com