
| A. | NaHSO4 | B. | NaHSO3 | C. | Al2(SO4)3 | D. | CH3COOH |
分析 常温下溶液中氢离子浓度越大,溶液酸性越强,硫酸氢钠在溶液中完全电离出氢离子,0.1mol/L的NaHSO4溶液中氢离子浓度为0.1mol/L,其酸性最强,其它物质氢离子浓度都较小,据此进行解答.
解答 解:A.0.1mol/L的NaHSO4溶液中,硫酸氢钠完全电离,氢离子浓度为0.1mol/L;
B.NaHSO3在溶液中部分电离出氢离子,溶液呈酸性,但氢离子浓度小于0.1mol/L;
C.Al2(SO4)3溶液中铝离子部分水解,溶液呈弱酸性,但氢离子浓度小于0.1mol/L;
D.CH3COOH为弱酸,在溶液中部分电离出氢离子,则0.1mol/L的CH3COOH溶液中氢离子浓度小于0.1mol/L;
氢离子浓度越大,溶液酸性越强,根据分析可知酸性最强的为NaHSO4,
故选A.
点评 本题考查溶液酸性强弱比较,题目难度不大,明确溶液酸性与氢离子浓度的关系为解答关键,注意掌握强弱电解质的概念及盐的水解原理,试题培养了学生的灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯气和明矾都能用于自来水的杀菌消毒 | |
| B. | 常温下,浓硫酸和浓硝酸都能用铜制容器盛装 | |
| C. | 钢铁设备连接锌块或电源正极都可防止其腐蚀 | |
| D. | 酸雨主要是由人为排放的硫氧化物和氮氧化物等转化而成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在25℃、1.01×105Pa时,11.2L氮气所含的原子数目为NA | |
| B. | 常温下,1L0.1mol/L的Na2CO3溶液中含有的离子总数为0.3NA | |
| C. | 钠在空气中燃烧可生成多种氧化物,23g钠充分燃烧时转移电子数为1NA | |
| D. | 1molP4和1molCH4中含有的共价健数均为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向漂白粉溶液中通入适量CO2以增强溶液的漂白性 | |
| B. | 将甲烷和氯气光照后的混合物通过饱和食盐水以获得纯净的一氯甲烷 | |
| C. | 滴定实验前用待测溶液润洗锥形瓶以减小实验误差 | |
| D. | 配制硝酸亚铁溶液时,将硝酸亚铁溶解在稀硝酸中再加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.02mol | B. | 0.03mol | C. | 0.05mol | D. | 0.17mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
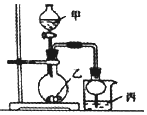
| 实验 | 试剂甲 | 试剂乙 | 试剂丙 | 丙中的现象 |
| A | 浓硫酸 | Na2SO3 | 紫色石蕊试液 | 溶液先变红红褪色 |
| B | 浓盐酸 | KMnO4 | 淀粉-Kl溶液 | 溶液变蓝 |
| C | 稀盐酸 | CaCO3 | BaCl2溶液 | 有白色沉淀生成 |
| D | 浓氨水 | CaO | AlCl3溶液 | 先生成白色沉淀然后沉淀溶解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com