
【题目】据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
(1)锌和镉位于同副族,而锌与铜相邻。现有 4 种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10。失去1个电子需要的能量由大到小排序是______(填字母)。
A.④②①③ B.④②③① C.①②④③ D.①④③②
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是_______。在硫的化合物中,H2S、CS2都是三原子分子,但它们的键角(立体构型)差别很大,用价层电子对互斥理论解释:_________;用杂化轨道理论解释:_________。
(3)Cd2+与NH3等配体形成配离子。[Cd(NH3)4]2+中2个NH3被2个Cl-替代只得到1种结构,它的立体构型是___________。1 mol [Cd(NH3)4]2+含___________mol σ键。
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为__________。
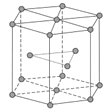
(5)锆晶胞如图所示,1个晶胞含_______个Zr原子;这种堆积方式称为__________。
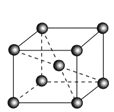
(6)镉晶胞如图所示。已知:NA是阿伏加德罗常数的值,晶体密度为 d g·cm-3。在该晶胞中两个镉原子最近核间距为______nm(用含NA、d的代数式表示),镉晶胞中原子空间利用率为________(用含π的代数式表示)。
【答案】A S原子半径小于Te,H-S键的键能较大 H2S分子中S原子价层有2个孤电子对,孤电子对对成键电子对排斥力大于成键电子对之间排斥力,所以键角较小;CS2分子中C原子价层没有孤电子对,成键电子对之间排斥力相同且较小 H2S中S采用sp3杂化,CS2中C采用sp杂化 正四面体 16 AsBr3>AsCl3>AsF3 6 六方最密堆积 ![]()
![]()
【解析】
(1)电离能大小与原子的外围电子构型有关,具有稳定构型的元素,电离能较大。而同一元素电离能满足:I1<I2<I3<I4。锌原子的第一电离能大于铜原子第一电离能,有①>③;铜的第二电离能大于锌的第二电离能,有④>②。锌的第二电离能大于第一电离能,②>①。故选A。答案为:A;
(2)从原子半径、键能角度分析气态氢化物的热稳定性。原子半径:r(S)<r(Te),键能:H-S>H-Te,所以H2S较稳定。H2S分子中S原子价层有2个孤电子对,孤电子对对成键电子对排斥力大于成键电子对之间排斥力,所以键角较小;CS2分子中C原子价层没有孤电子对,成键电子对之间排斥力相同,呈直线形最稳定,键角较大。从杂化轨道角度解释,H2S中S采用sp3杂化,CS2中C采用sp杂化。答案为:S原子半径小于Te,H–S键的键能较大;H2S分子中S原子价层有2个孤电子对,孤电子对对成键电子对排斥力大于成键电子对之间排斥力,所以键角较小;CS2分子中C原子价层没有孤电子对,成键电子对之间排斥力相同且较小;H2S中S采用sp3杂化,CS2中C采用sp杂化;
(3)[Cd(NH3)4]2+中2个NH3被2个Cl替代只得到1种结构,说明Cd2+采用sp3杂化,呈正四面体结构。配位键也是σ键。1 mol [Cd(NH3)4]2+含16 mol σ键。答案为:正四面体;16;
(4)它们都是分子晶体,相对分子质量越大,范德华力越大,熔点越高。故熔点排序为AsBr3>AsCl3>AsF3。答案为:AsBr3>AsCl3>AsF3;
(5)在六棱柱中,12个原子位于顶点、2个原子位于面心,3个原子位于体内。1个六棱柱含6个原子。这种堆积方式叫六方最密堆积。答案为:6;六方最密堆积;
(6)图2为体心立方堆积,3个镉原子位于体对角线且相切,1个晶胞含2个镉原子。设晶胞参数为a,d=![]() ,a=
,a=![]() nm。设两镉原子最近核间距为x,(2x)2=3a2,x=
nm。设两镉原子最近核间距为x,(2x)2=3a2,x=![]() nm。设镉原子半径为r,则r=
nm。设镉原子半径为r,则r=![]() nm,φ=
nm,φ=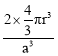 =
=![]() 。答案为:
。答案为:![]() ;
;![]() 。
。


科目:高中化学 来源: 题型:
【题目】科学家模仿植物的光合作用,开发出了利用太阳光、水及二氧化碳(CO2)合成甲烷(CH4)的人工光合系统,其工作原理如图所示。下列说法错误的是( )
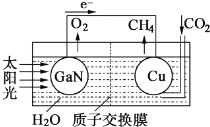
A. GaN为负极,Cu为正极 B. 该装置中只存在两种能量的转化
C. GaN电极的电极反应式为2H2O-4e-=4H++O2↑ D. 该装置工作时,H+向Cu电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为________。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为__________,C的元素符号为____________;B的外围电子的轨道表示式为___________。
(3)D元素的正三价离子的3d轨道为半充满,D的元素符号为________________,其基态原子的电子排布式为________________________。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为________,其基态原子的电子排布式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。
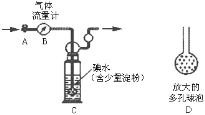
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是:_________。
(2)洗气瓶C中的溶液可以酸性高锰酸钾溶液替代,请写出离子方程式:________。
(3)本实验的关键在于关闭气体流量计的时机,应当在什么时候关闭活塞A____________
乙方案:实验步骤如以下流程图所示:
![]()
(4)写出步骤①中反应的化学方程式_________。
(5)如何判断步骤②中沉淀是否完全的方法___________。
(6)经测定当通过的尾气体积为67.2L(已换算成标准状况)时,最终得到固体质量为4.66g,则该尾气中二氧化硫含量(体积分数)为__________(保留到0.01%)
丙方案:将乙中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与方案乙相同。
(7)你认为丙方案________(填是或否)合理,说明理由:___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以二氧化碳为原料制备尿素工艺被广泛研究。其反应机理为:
反应Ⅰ:CO2(g)+2NH3(g)NH2COONH4(l) H1=-117.2 kJ·mol1
反应Ⅱ:NH2COONH4(l)NH2CONH2(l)+H2O(l) H2= +15.0 kJ·mol1
(1)反应Ⅰ平衡常数K的表达式为_____________。
(2)由CO2(g)和NH3(g)合成尿素NH2CONH2(l)的热化学方程式是__________。
(3)在恒容容器中按物质的量之比1∶2通入CO2和NH3,下列不能说明合成尿素反应达平衡状态的是_________。
A.容器中气体平均相对分子质量不再变化
B.容器中气体密度不再变化
C.NH3的体积分数不再变化
D.容器内压强不再变化
(4)通过实验发现,其他条件不变时,改变NH3、CO2的物质的量之比可增加尿素的产率,如图为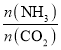 与尿素产率的关系曲线。通过曲线可知:______________过量对尿素产率的影响比较小。若在固定容器中按
与尿素产率的关系曲线。通过曲线可知:______________过量对尿素产率的影响比较小。若在固定容器中按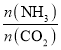 等于3.0通入CO2和NH3,则合成尿素反应达平衡后,混合气体中CO2的物质的量分数为________(精确到0.1%)。
等于3.0通入CO2和NH3,则合成尿素反应达平衡后,混合气体中CO2的物质的量分数为________(精确到0.1%)。
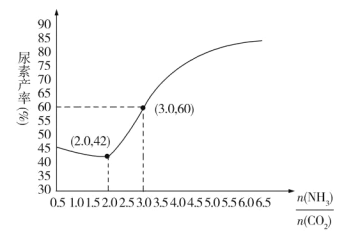
(5)探究发现,温度、压强、n(H2O)条件对合成尿素反应的影响如图1、图2,根据图像回答下列问题:
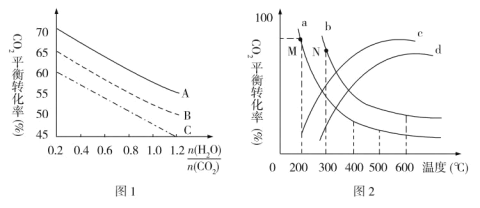
①其他条件不变时,对于合成尿素的反应,若通入CO2物质的量一定,按三种投料比[分别为 3.0、3.5、4.0]投料时,得到如图1的横轴对CO2的平衡转化率的影响曲线。曲线A对应的投料比是________。
②图2中a、b、c、d 四条曲线中的两条代表压强分别为20 MPa、25 MPa时CO2平衡转化率曲线,其中表示20MPa的是_________(填字母)。在实际生产中采用图2中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的主要原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】轴烯(Radialene)是一类独特的环状烯烃,其环上每一个碳原子都接有一个双键,含n元环的轴烯可以表示为[ n]轴烯,如下图是三种简单的轴烯。下列有关说法不正确的是
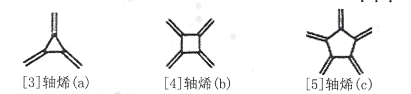
A.a分子中所有原子都在同一个平面上B.b能使酸性KMnO4溶液褪色
C.c与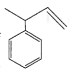 互为同分异构体D.轴烯的通式可表示为C2nH2n(n≥3)
互为同分异构体D.轴烯的通式可表示为C2nH2n(n≥3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水:Al3++4OH-=![]() +2H2O
+2H2O
B.氢氧化钡溶液与稀硫酸反应:Ba2++![]() =BaSO4↓
=BaSO4↓
C.碳酸钙与盐酸反应:![]() +2H+=H2O+CO2↑
+2H+=H2O+CO2↑
D.金属钠与水反应:2Na+2H2O=2Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂生产废液中含有大量的Cu2+ 、Fe3+、Fe2+ 、![]() 。某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾(FeSO4·7H2O):
。某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾(FeSO4·7H2O):

请回答以下问题:
(1)操作1和操作2的名称是________。
(2)废液中加过量铁时发生反应的离子方程式为_______________、________________。
(3)合并溶液1和溶液2后,系列操作3包含__________、____________、过滤等操作。
(4)若使用得到的绿矾晶体制备净水剂Fe2(SO4)3溶液,除在绿矾中加入适量稀硫酸外,还需要加入____(填标号)。
①稀H2SO4 ②Cl2 ③H2O2 ④Fe粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界的氮循环如下图所示,下列说法不正确的是( )

A.①中N2与O2反应生成NO
B.②中合成氨属于人工固氮
C.③中氮元素只被氧化
D.氧元素参与了氮循环
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com