
 .
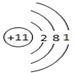
.分析 (1)与Ne原子电子层结构相同的+1价阴离子是钠离子;
(2)1个甲烷(CH4)分子含有10个电子,1个铵根离子含有10个电子,所以等物质的量的甲烷(CH4)与铵根所含的电子数相等;
(3)根据n=$\frac{m}{M}$计算出氨气的物质的量,再根据N=nNA计算出含有氨气分子数及含有的氢原子数目,结合甲烷的分子结构求出甲烷的物质的量,根据V=nVm求甲烷的体积.
解答 解:(1)与Ne原子电子层结构相同的+1价阴离子是钠离子,所以钠原子的结构示意图为 ,故答案为:
,故答案为: ;
;
(2)1个甲烷(CH4)分子含有10个电子,1个铵根离子含有10个电子,所以等物质的量的甲烷(CH4)与铵根所含的电子数相等,所以等物质的量的甲烷(CH4)与铵根所含的电子数之比为1:1,故答案为:1:1;
(3)氨气的相对分子质量是17,其摩尔质量是17g/mol,则3.4g氨气的物质的量为:n(NH3)=$\frac{3.4g}{17g/mol}$=0.2mol,所以含有氨气的分子数为:N(NH3)=nNA=0.2×NA=0.2NA=1.024×1023,含有氢原子的数目为:N(H)=3N(NH3)=0.6NA,与氨气含有H原子数目相等的CH4的物质的量$\frac{0.6{N}_{A}}{4}$=0.15NA,故CH4的体积=0.15mol×22.4L/mol=3.36L,故答案为:1.024×1023;3.36.
点评 本题考查了有关物质的量的计算,题目难度不大,注意掌握物质的量与阿伏伽德罗常数、摩尔质量、物质的量等物理量之间的转化关系,灵活运用公式是解答的关键.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| A. | 自然界中不存在游离态的硫 | |
| B. | 二氧化碳的排放会导致酸雨的产生 | |
| C. | 二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性 | |
| D. | 浓硫酸可用来干燥SO2、CO、Cl2等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.8 g | B. | 5.4 g | C. | 6.0 g | D. | 6.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠在空气中燃烧,生成淡黄色的氧化钠粉末 | |
| B. | 钠是一种强还原剂,可以把钛从其盐溶液中置换出 | |
| C. | 将灼热的铜丝放入盛有氯气的集气瓶中,生成棕黄色的雾 | |
| D. | Fe(OH)3胶体具有吸附性,能吸附水中的悬浮颗粒并沉降,因而可用于净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用大理石跟稀盐酸制取二氧化碳2H++CO32-═CO2↑+H2O | |
| B. | 氯气与水反应 Cl2+H2O═2H++Cl-+ClO- | |
| C. | 氧化铝跟氢氧化钠溶液反应Al2O3+OH-═AlO2-+H2O | |
| D. | 金属钠跟水反应2Na+2H2O═2Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H12O6(葡萄糖aq)+6O2$\stackrel{酶}{→}$6CO2+6H2O | |
| B. | CH3COOH+KOH?CH3COOK+H2O | |
| C. | A+B?C+D;△H<0 | |
| D. | 反应物所具有的总能量小于生成物所具有的总能量的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2的水溶液能导电,所以SO2是电解质 | |
| B. | 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 | |
| C. | 所有的共价化合物都是弱电解质,所有的离子化合物都是强电解质 | |
| D. | 强酸、强碱及大部分盐类都属于强电解质,弱酸、弱碱都属于弱电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com