
分析 (1)配制450mL稀盐酸,实际上配制的是500mL 0.1mol/L的稀盐酸,根据配制过程中溶质HCl的物质的量不变计算出需要浓盐酸的体积;
(2)根据计算出的浓盐酸体积选用量筒;
(3)根据配制一定物质的量浓度的溶液步骤判断使用的仪器;
(4)根据c=$\frac{n}{V}$可知,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化:若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.
解答 解:(1)用12mol•L-1的浓盐酸配制0.10mol•L-1的稀盐酸450mL,需要选用规格为500mL 的容量瓶,则需要该浓盐酸的体积为:$\frac{0.1mol/L×0.5L}{12mol/L}$≈0.0042L=4.2mL,
故答案为:4.2;
(2)需要量取4.2mL浓盐酸,应该选用10mL的量筒,
故答案为:D;
(3)配制500mL 0.1mol/L的稀盐酸的步骤为:计算、量取、稀释、冷却、转移、洗涤、定容等,则使用的仪器为:量筒、烧杯、玻璃棒、胶头滴管和500mL容量瓶等,
故答案为:胶头滴管;500mL容量瓶;
(4)A.用量筒量取浓盐酸时仰视,量取的浓盐酸体积偏大,配制的溶液浓度偏高,故A正确;
B.容量瓶定容时,仰视容量瓶刻度线,加入的蒸馏水体积偏大,配制的溶液浓度偏低,故B错误;
C.容量瓶中加水超过刻度线,吸出一部分水,配制的溶液体积偏大,溶液浓度偏低,故C错误;
D.摇匀后液面下降,补充水,导致配制的溶液体积偏大,溶液浓度偏低,故D错误;
故答案为:A.
点评 本题考查了配制一定物质的量浓度的溶液的方法,该题是中等难度的试题,试题基础性强,贴近高考;该题难易适中,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力;该题的难点在于误差分析,注意明确误差分析的方法.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 等体积的0.010mol/LB(OH)2溶液与0.010mol/LH2SO4溶液恰好完全反应 | |
| B. | 0.010mol/LB(OH)2溶液能使红色石蕊试液变蓝 | |
| C. | 0.010mol/LBCl2溶液呈酸性,0.010mol/LB2CO3溶液呈中性 | |
| D. | 0.010mol/LB(OH)2溶液能够与NH4Cl反应生成NH3(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
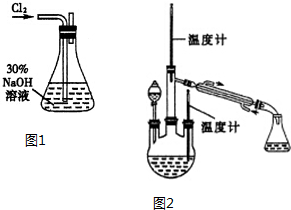 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H20).
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H20).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的稳定性:H2O>H2S>SiH4 | |
| B. | 离子半径:Cl->O2->Mg2+ | |
| C. | 物质酸性:H3PO4>H2SO4>HClO4 | |
| D. | 熔点:KCl>K |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含2molH2SO4的浓硫酸与足量铜反应生成1molSO2 | |
| B. | 硫粉在过量的氧气中燃烧可以生成SO3 | |
| C. | 铜与稀硝酸反应生成0.5molNO气体,则转移电子数为NA | |
| D. | 可用品红溶液或酸性KMnO4溶液鉴别 CO2和SO2,不可用澄清石灰水鉴别 CO2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
| A. | 放出248 kJ 热量 | B. | 吸收248 kJ 热量 | C. | 放出183kJ 热量 | D. | 吸收183 kJ 热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
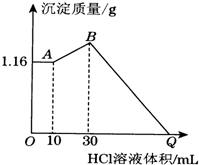 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
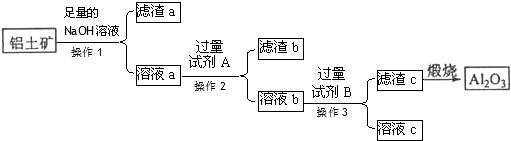
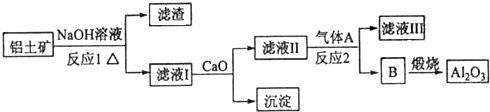
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com