
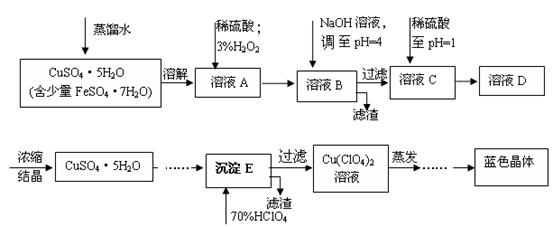
| 离子 | 溶液pH值 | |
| 开始沉淀 | 沉淀完全 | |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Cu2+ | 5.2 | 6.4 |
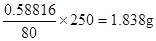 ,所以纯度是1.8385÷2×100%=91.9%,所以相对误差是(91.9%-93.2%)÷93.2%×100%=-1.4%。
,所以纯度是1.8385÷2×100%=91.9%,所以相对误差是(91.9%-93.2%)÷93.2%×100%=-1.4%。

科目:高中化学 来源:不详 题型:单选题
| A.⑤②③①④ | B.④①③②⑤ |
| C.③②①⑤④ | D.③②④①⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加热氯化铁溶液的颜色变深 |
| B.CaCO3的饱和溶液pH约为9.3 |
| C.0.1 mol/L AlCl3溶液中c(Al3+)<0.1 mol/L |
| D.NaHCO3做发酵粉时加入柠檬酸后效果更好 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
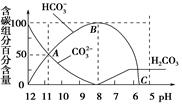
| A.0.1 mol/L Na2CO3溶液中c(OH-)-c(H+)=2c(H2CO3)+c(HCO3-) |
| B.在A点c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| C.常温下CO2饱和溶液的pH约为5.6 |
| D.0.05 mol/L NaHCO3溶液的pH=8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.甲同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的。 |
| B.乙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的。 |
| C.丙同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的。 |
| D.丁同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若①正确,则溶液中溶质一定为NH4Cl |
| B.若③正确,则溶液中c(NH3·H2O) + c(NH4+)>c(Cl—) |
| C.若④正确,且盐酸和氨水体积相等,则盐酸中c(H+)等于氨水中c(OH—) |
| D.溶质不同时,上述四种关系式均可能成立 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若混合后溶液的pH=7,则c(M+)=c(C1-) |
| B.若a=2b,则c (M+) > c(C1-) > c (MOH) > c(OH-) > c(H+) |
| C.若b=2a,则c(C1-) > c(M+) > c(H+) > c(OH-) |
| D.若混合后溶液满足c(H+)=c(OH-)+c(MOH),则可推出a=b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com