
 2NH3(g) ΔH=-92kJ·mol-1
2NH3(g) ΔH=-92kJ·mol-1 ,原因是
,原因是  N键、1mol H
N键、1mol H H键需要吸收的能量为:946 kJ、436 kJ,则破坏1mol N
H键需要吸收的能量为:946 kJ、436 kJ,则破坏1mol N H键需要吸收的能量为 kJ。
H键需要吸收的能量为 kJ。 ΔH1=+67.7 kJ/mol
ΔH1=+67.7 kJ/mol 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题

| A.蒸馏水 | B.氯化钠固体 | C.氯化钠溶液 | D.浓盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
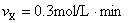
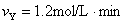

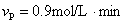
| A.甲 | B.乙 | C.丙 | D.丁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 xC(g)+2D(g),2min后达到平衡时生成1.6molC,又测得反应速率v(D)=0.2mol/(L·min)。下列说法正确的是( )
xC(g)+2D(g),2min后达到平衡时生成1.6molC,又测得反应速率v(D)=0.2mol/(L·min)。下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.降低压强能加快反应速率 |
| B.使用适当催化剂可以加快反应速率 |
| C.升高温度能加快反应速率 |
| D.改变压强对反应速率没有影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.四种物质的浓度相等,则一定达到了该反应的限度 |
| B.各物质的浓度不再发生变化时,则达到化学反应的限度 |
| C.升高反应的温度,则反应速率减慢 |
| D.使用催化剂,能改变反应限度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com