
| A. | 制备乙酸乙酯时将产生的蒸气导入饱和碳酸钠溶液:CO32-+2H+═CO2↑+H2O | |
| B. | 用惰性电极电解饱和食盐水:2Cl-+2H+$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| C. | 向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2 | |
| D. | 饱和Ca(OH)2溶液中加入少量NaHCO3溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
分析 A.醋酸为弱酸,应保留化学式;
B.水为弱电解质,应保留化学式;
C.由电子守恒可知,0.4mol亚铁离子全部被氧化,0.2mol溴离子被氧化;
D.碳酸氢钠少量,反应生成碳酸钙、氢氧化钠和水.
解答 解:A.醋酸与碳酸钠反应生成醋酸钠和二氧化碳、水,离子方程式:CO32-+2HAc=2Ac-+CO2↑+H2O,故A错误;
B.用惰性电极电解饱和食盐水,离子方程式:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-,故B错误;
C.由电子守恒可知,0.4mol亚铁离子全部被氧化,0.2mol溴离子被氧化,发生的离子反应为:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2,故C错误;
D.饱和Ca(OH)2溶液中加入少量NaHCO3溶液,离子方程式:Ca2++OH-+HCO3-═CaCO3↓+H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意反应物用量对反应的影响.


科目:高中化学 来源: 题型:解答题
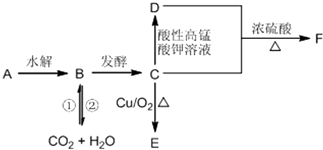
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 第二周期ⅣA族 第二周期ⅢA族 第七周期ⅣA族 | |
| B. | 第四周期ⅡA族 第二周期ⅢA族 第七周期ⅣA族 | |
| C. | 第二周期ⅣA族 第三周期ⅡA族 第四周期ⅦA族 | |
| D. | 第二周期ⅣA族 第三周期ⅡA族 第四周期ⅣA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br2、CO2、H2O、HBr | B. | CO2、O2、H2S、HCl | ||
| C. | Na2O2、S8、CO2、H2O | D. | CO2、H2S、H2O、HI |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
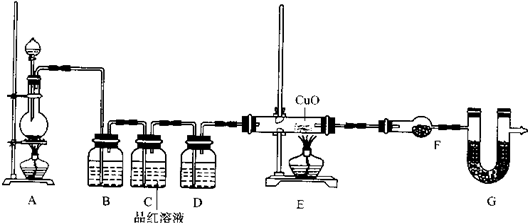
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有离子键的化合物一定是离子化合物 | |
| B. | 非金属元素形成的单质中,一定有非极性共价键 | |
| C. | 两种元素组成的分子中一定只有极性键 | |
| D. | 均由非金属元素形成的化合物不可能是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol/L AlCl3溶液中含有的离子数是0.4NA | |
| B. | 3.9g Na2O2吸收足量的CO2时转移的电子数是0.05NA | |
| C. | 1L 1.0mol/L NaCl溶液中含有NA个NaCl分子 | |
| D. | 标准状况下,1.12L的SO3所含的原子数是0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com