
【题目】实验室可用环己醇制备环己酮,使用的氧化剂可以是次氯酸钠、重铬酸钾等。

已知:环己醇沸点:160.8℃,微溶于水;
环己酮沸点:155.6℃,微溶于水;
醋酸沸点117.9℃,和水以任意比例互溶。
下列装置分别是产品的合成装置和精制装置示意图:
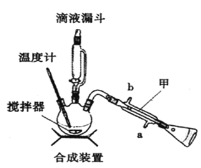
合成实验过程如下:
向装有搅拌器、滴液漏斗和温度计的三颈烧瓶中依次加入5.2mL环己醇和25mL冰醋酸。开动搅拌器,将40mL次氯酸钠溶液逐渐加入到反应瓶中,并使瓶内温度维持在30~35℃,用磁性搅拌器搅拌5min。然后,在室温下继续搅拌30min后,在合成装置中再加入30mL水、3g氯化铝和几粒沸石,加热蒸馏至馏出液无油珠滴出为止。回答下列问题:
(1)在合成装置中,甲装置的名称是_____________。
(2)三颈烧瓶的容量为_____________(填“50mL"、“100mL”或“250mL")。
(3)滴液漏斗具有特殊的结构,主要目的是_____________。
(4)蒸馏完成后,向馏出液中分批加入无水碳酸钠至反应液呈中性为止,其目的是_____________。然后加入精制食盐使之变成饱和溶液,将混合液倒入_____________中,分离得到有机层。
(5)用如图对粗产品进行精制,蒸馏收集_____________℃的馏分。
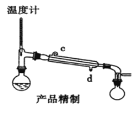
(6)检验环己酮是否纯净,可使用的试剂为_____________。
A.重铬酸钾溶液B.金属钠C.新制的氢氧化铜悬浊液D.醋酸溶液
【答案】直形冷凝管 250mL 平衡压强,使所加液体能顺利滴入三颈烧瓶中 除去产品中混有的醋酸杂质 分液漏斗 155.6 AB
【解析】
根据整个反应过程中所加液体的总体积大于100mL可知,反应需选250 mL的三颈烧瓶;为了使所加液体能顺利滴入三颈瓶中采用滴液漏斗;在装有搅拌器、滴液漏斗和温度计的三颈烧瓶中,由环己醇和冰醋酸、次氯酸钠等物质加热反应后蒸馏得到环己酮的粗产品;因环己酮沸点为155.6℃,故可收集155.6℃时的馏出液,但由于醋酸沸点为117.9℃,所以馏出液中含有杂质醋酸,为了纯化产物,因醋酸能和水以任意比例互溶,且与碳酸钠反应后的产物不溶于有机物溶液中,故向馏出液中分批加入无水碳酸钠至反应液呈中性为止以除去产品中混有的醋酸杂质。由于有机物在盐溶液中的溶解度小,盐溶液能减少有机物的溶解损失,所以加入精制食盐使之变成饱和溶液,将混合液倒入分液漏斗中,分离即可得到有机层。
(1)在合成装置中,甲起冷凝作用,甲装置的名称是直形冷凝管;
(2) 三颈烧瓶中依次加入5.2mL环己醇和25mL冰醋酸,将40mL次氯酸钠溶液逐渐加入到反应瓶,在合成装置中再加入30mL水、3g氯化铝和几粒沸石,可知溶液的总体积大于100mL,所以选250 mL的三颈烧瓶;
(3)滴液漏斗具有特殊的结构,使三颈瓶内的压强与漏斗内的压强相等,使所加液体能顺利滴入三颈瓶中;
(4)Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑,馏出液中分批加入无水碳酸钠至反应液呈中性为止,其目的是将反应混合物中醋酸变成醋酸钠,便于分离;产品在精制饱和食盐溶液中溶解度小,有利于分层,用分液漏斗可将其分离出来;
(5)环己酮的沸点:155.6℃,所以收集155.6℃的馏分;
(6)A.环己醇能被重铬酸钾溶液氧化,重铬酸钾溶液变成绿色,若两者混合不显示绿色,则说明产品中不含杂质环己醇,A符合题意;
B.环己醇中的醇羟基能与钠发生置换反应,生成H2,若两者混合不产生氢气则说明产品中不含杂质环己醇,B符合题意;
C.新制的氢氧化铜悬浊液与两者均不反应,无法检验环己酮是否纯净,C不符合题意;
D.醋酸本来就是产物中所含的杂质,不能用其来检验环己酮是否纯净,D不符合题意;
答案选AB。


科目:高中化学 来源: 题型:
【题目】多尺度复杂化学系统模型可以用量子化学计算小区间内(如生物固氮时固氮酶中)的化学反应。
(1)固氮酶有铁蛋白和钼铁蛋白两种,它们不仅能够催化N2还原成NH3,还能将环境底物乙炔催化还原成乙烯。
①乙炔是__________(填“非极性”或“极性”)分子。
②碳负离子CH3-的立体构型为____________。
③根据等电子原理,NO+的电子式为________________。
(2)钒可用于合成电池电极,也可用于人工合成二价的钒固氮酶(结构如图a)。
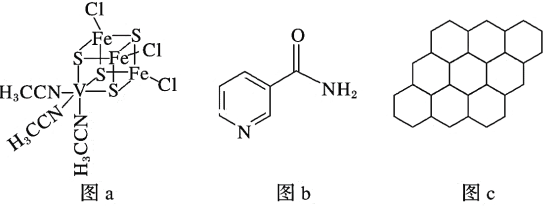
①V2+基态时核外电子排布式为____________________________________________。
②钒固氮酶中钒的配位原子有_____________________________(填元素符号)。
(3)烟酰胺(结构如图b)可用于合成光合辅酶NADPH,烟酰胺分子中氮原子的杂化轨道类型有_______________________,1 mol该分子中含σ键的数目为________。
(4)12 g石墨烯(结构如图c)中含有的正六边形数目约为________;请你预测硅是否容易形成类似石墨烯的结构,并说明理由:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)下列六种生活中常见物质:
①食盐 ②食用油 ③靑霉素 ④鸡蛋 ⑤西红柿 ⑥塑料
按要求用物质序号填空:
作调味剂的是___________;作抗生素的是___________;富含蛋白质的是___________;富含维生素的是___________;富含油脂的是___________;属于合成材料的是___________。
(2)一个体重50 kg的健康人,体内约含有2 g铁,这2 g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+, 有利于人体吸收。
i.在人体中进行Fe2+ ![]() Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
Fe3+的转化时,①中的Fe2+作________ (填“氧化剂”或“还原剂”),②中的Fe3+作________ (填“氧化剂”或“还原剂”)。
ii.服用维生索C,可使食物中的Fe3+还原成Fe2+这句话指出,维生素C在这一反应中作 ____________(填“氧化剂”或“还原剂”)
iii.市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸 (HC1)的作用下转化成亚铁盐。此反应的离子方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】建造舰船需要大量的新型材料,舰船的甲板也要耐高温且外壳要耐腐蚀,而镍铬铁合金就是具有高强度、耐高温、耐腐蚀等优良性能的特种钢,这类特种钢中含有碳、硅、氧、氮、磷等元素。
(1)保铬钢抗腐蚀性能强,![]() 基态原子的价电子排布_________,为铬元素在周期表中_________区。
基态原子的价电子排布_________,为铬元素在周期表中_________区。
(2)![]() 能形成多种配离子,如
能形成多种配离子,如![]() 、
、![]() 和
和![]() 等,
等,![]() 中心原子的配位数是_________,与
中心原子的配位数是_________,与![]() 互为等电子体的分子为_________。
互为等电子体的分子为_________。
(3)舰船甲板涂有一层耐高温的材料聚硅氧烷结构如图所示,其中![]() 原子杂化方式为________杂化。
原子杂化方式为________杂化。
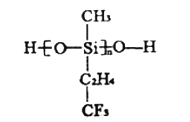
(4)碳和硅可化合成碳化硅,![]() 晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,但是碳化硅的熔点低于金刚石,原因是_________。
晶体具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,但是碳化硅的熔点低于金刚石,原因是_________。
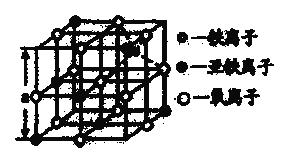
(5)铁的氧化物之一是![]() ,从
,从![]() 中取出的能体现其晶体结构的一个立方体,则晶体中的离子是否构成了面心立方最密堆积?________(填“是”或“否”);该立方体是不是
中取出的能体现其晶体结构的一个立方体,则晶体中的离子是否构成了面心立方最密堆积?________(填“是”或“否”);该立方体是不是![]() 的晶胞?_________(填“是”或“否”);立方体中铁离子处于氧离子围成的_________(填空间结构)空隙;根据上图计算
的晶胞?_________(填“是”或“否”);立方体中铁离子处于氧离子围成的_________(填空间结构)空隙;根据上图计算![]() 晶体的密度为_________
晶体的密度为_________![]() 。(图
。(图![]() ,计算结果保留两位有效数字)
,计算结果保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
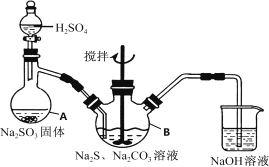
【题目】硫代硫酸钠(![]() )可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等.它易溶于水,难溶于乙醇,受热易分解,在酸性溶液中不能稳定存在.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如下图:
)可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等.它易溶于水,难溶于乙醇,受热易分解,在酸性溶液中不能稳定存在.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如下图:
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的![]() 气体较均匀地通入
气体较均匀地通入![]() 和
和![]() 的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
②直至析出的浑浊不再消失,并控制溶液的![]() 接近7时,停止通入
接近7时,停止通入![]() 气体。
气体。
③趁热过滤,将滤液加热浓缩,冷却析出![]() 。
。
④再经过滤、洗涤、干燥,得到所需的产品。
(1)仪器A的名称是_________。
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液![]() ,请用离子方程式表示原因_________。
,请用离子方程式表示原因_________。
(3)写出三颈烧瓶B中制取![]() 反应的总化学反应方程式_________。
反应的总化学反应方程式_________。
(4)为了验证固体硫代硫酸钠工业产品中含有碳酸钠,选用下列装置进行实验:
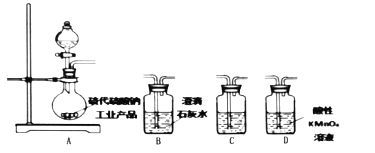
①实验装置的连接顺序依次_________(填装置的字母代号,各装置限用一次),装置C中的试剂为_________。
②能证明固体中含有碳酸钠的实验现象是_________。
③若要检验固体硫代硫酸钠工业产品中含有![]() ,需先加水配成稀溶液,再依次加入的试剂为_________、_________和品红溶液。
,需先加水配成稀溶液,再依次加入的试剂为_________、_________和品红溶液。
(5)![]() 常用作脱氯剂,在溶液中易被
常用作脱氯剂,在溶液中易被![]() 氧化成
氧化成![]() ,该反应的离子方程式为_________。
,该反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸钠可用于制备高氯酸。以精制盐水等为原料制备高氯酸钠晶体(NaClO4·H2O)的流程如图:
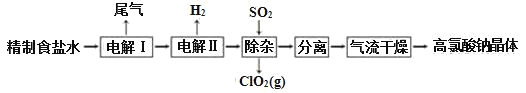
(1)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为______。
A.先加NaOH,后加Na2CO3,再加钡试剂
B.先加NaOH,后加钡试剂,再加Na2CO3
C.先加钡试剂,后加NaOH,再加Na2CO3
除去盐水中的Br-可以节省电解过程中的电能,其原因是_____。
(2)“电解Ⅰ”的目的是制备NaClO3溶液,产生的尾气除H2外,还含有_____(填化学式)。“电解Ⅱ”的化学方程式为____。
(3)“除杂”的目的是除去少量的未反应的NaClO3杂质,该反应的离子方程式为_____。“气流干燥”时,温度控制在80~100℃,温度不能过高的原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,下列叙述正确的是( )
A.在周期表金属与非金属分界处寻找用于研制新农药的元素
B.H2、D2、T2互为同位素
C.如图所示实验可证明元素的非金属性:Cl>C>Si
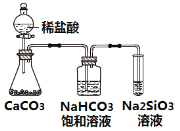
D.用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素
A. 在自然界中只以化合态的形式存在
B. 单质常用作左半导体材料和光导纤维
C. 最高价氧化物不与酸反应
D. 气态氢化物比甲烷稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化亚铁易被氧化,制取过程要隔绝空气。现用铁屑、稀硫酸、氢氧化钠溶液制备氢氧化亚铁并观察其颜色,改进装置如下:
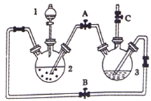
(1)稀硫酸应放在___(填写仪器名称)中。
(2)本实验通过关闭开关___、打开开关___,将仪器中的空气排尽后,后续实验就可观察到氢氧化亚铁的颜色。
(3)在FeSO4溶液中加入(NH4)2SO4固体可制备莫尔盐晶体[(NH4)2SO4·FeSO4·6H2O](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
①为洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是___。
a.用冷水洗 b.先用冷水洗,后用无水乙醇洗
c.用30%的乙醇溶液洗 d.用90%的乙醇溶液洗
②为了测定产品的纯度,称取ag产品溶于水,配制成500mL溶液。每次取待测液20.00mL,用浓度为bmol/L的酸性KMnO4溶液滴定,实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗酸性高锰酸钾溶液体积/mL | 20.02 | 19.98 | 20.52 |
滴定过程中发生反应的离子方程式为___。滴定终点的现象是___。
通过实验数据计算的该产品纯度为___(用字母a、b表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com