
常温下,某无色透明的溶液中,下列各组离子能够大量共存的是
A.H+、Na+、Cl-、CO32- B.Ba2+、Na+、SO42-、Cl-
C.MnO4- 、K+ 、I- 、H+ D.Mg2+ 、Cl-、NO3- 、H+
科目:高中化学 来源:2015-2016学年江西省高二上第二次月考化学试卷(解析版) 题型:选择题
2013年1月全国大部分地区出现雾霾天气,北京PM2.5浓度达993,系中国有该监测数据以来最高的一次。“拯救人类的最后机会”只有节能减排,下列属最有希望的新能源是
①天然气 ②煤 ③石油 ④水能 ⑤太阳能 ⑥地热能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.③④⑤⑥ D.除①②外
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南宁远一中、祁阳一中高二上第二次联考化学试卷(解析版) 题型:选择题
在一恒压密闭容器中充入1 mol NO2建立如下平衡:2 NO2 N2O4, 此时NO2的转化率为x%,在其他条件不变的条件下,再充入1 mol NO2,待新平衡建立时测得NO2的转化率为y%,则大小关系正确的是
N2O4, 此时NO2的转化率为x%,在其他条件不变的条件下,再充入1 mol NO2,待新平衡建立时测得NO2的转化率为y%,则大小关系正确的是
A.x < y B.x = y
C.x > y D.无法确定
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省枣阳市高一上学期期中考试化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列有关说法中不正确的是
A.标准状况下,22.4 L氦气含有NA个氦原子
B.20 g重水含有10 NA个电子
C.12.5 mL l6 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2 NA
D.1.6 g由氧气和臭 氧组成的混合物中含有氧原子的数目为0.1 NA
氧组成的混合物中含有氧原子的数目为0.1 NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省枣阳市高一上学期期中考试化学试卷(解析版) 题型:选择题
用NA代表阿伏加德罗常数,下列说法正确的是
A.14gC2H4和C4H8的混合气体中所含的共价键数为3NA
B.标准状况下,11.2L SO3所含的分子数为0.5NA
C.24g3H218O含有的中子数为12NA
D.0.1mol O22-所含的电子数为1.6NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省枣阳市高一上学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.在常温常压下,11.2 L N2含有的分子数为0.5NA
B.常温常压下1 mol Ne含有的原子数为NA
C.22.4L Cl2所含原子数为2NA
D.在同温同压下,相同体积的任何气体单质所含原子数相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:实验题
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x的值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
学习小组的同学设计了滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000 mol·L-1的KMnO4标准溶液进行滴定,达到终点时消耗了10.00mL。
请回答下列问题:
(1)滴定时,将酸性KMnO4标准液装在如图中的 (填“甲”或“乙”)滴定管中。

(2)本实验滴定达到终点的标志是 。
(3)通过上述数据,求得x= 。讨论:
①若滴定终点时俯视滴定管,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期半期考试化学试卷(解析版) 题型:填空题
铁及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)钢铁在潮湿的空气中发生吸氧腐蚀的正极反应式为 。
(2)生铁中含有一种铁碳化合物X(Fe3C),X在足量的空气中高温煅烧,生成有磁性氧化物Y,Y可溶于过量盐酸,形成黄绿色的溶液,写出Y与盐酸反应的化学方程式 。
(3)某炼铁废渣中含有大量CuS及少量铁的化合物,工业上以该废渣为原料生产CuCl2·H2O的工艺流程如下:
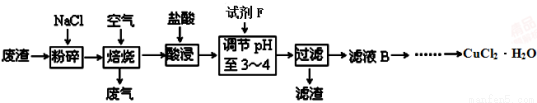
已知:Fe(OH)2、Fe(OH)3、Cu(OH)2沉淀完全时的pH值分别为9.7、3.3、6.4。
试回答下列问题:
①试剂F应选用 (填编号)。
A.Cl2 B.NaClO C.HNO3 D.浓硫酸
理由是 。
②为了获得晶体,对滤液B进行的操作是蒸发浓缩,趁热过滤,滤液经冷却结晶,过滤得到产品。分析有关物质的溶解度曲线(如图),“趁热过滤”得到的固体是 。

查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三上学期期中测试化学试卷(解析版) 题型:推断题
(I)A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:

(1)若B是淡黄色固体,②③反应均用到同一种液态氢化物。D物质常用于食品工业。写出④反应的化学方程式___________________________。
(2)若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。写出③反应的化学方程式______________。
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出④反应离子方程式________________________。
(4)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式________________________。
(5)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。写出④反应的离子方程式______________________________________________。
(II)在温度相同、体积均为1 L的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。已知:2SO2(g)+O2(g) 2SO3(g) ΔH =-98.3 kJ·mol-1。
2SO3(g) ΔH =-98.3 kJ·mol-1。
容 器 | 甲 | 乙 | 丙 |
反应物投入量 | 2 mol SO2、1 mol O2 | 2 mol SO3 | m mol SO2、n mol O2、p mol SO3 |
c(SO3) /mol·L-1 | 1.4 | 1.4 | 1.4 |
能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
SO2或SO3的转化率 | α1 | α2 | 12.5% |
则:α1+α2=_________________,p=________________mol,b+c=_______________kJ 。
(III)HA、H2B、H3C三种弱酸,根据“较强酸+较弱酸盐 较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:A.HA+HC2-(少量)
较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:A.HA+HC2-(少量) A-+H2C- B.H2B(少量)+2A-
A-+H2C- B.H2B(少量)+2A- B2-+2HA
B2-+2HA
C.H2B(少量)+H2C- HB-+H3C
HB-+H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中,酸性最强的是_____________。
(2)A-、B2-、C3-、HB-、H2C-、HC2-六种离子中,最易结合质子(H+)的是_________,最难结合质子的是____________。
(3)完成下列反应的离子方程式HA(过量)+C3-:________________________________。
(IV)在25下,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,反应平衡时溶液中c(NH4+) = c(Cl-),则溶液显______________(填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com