
| A、将142gNa2SO4溶于少量水后再稀释到100mL |
| B、1L溶液中含有142gNa2SO4 |
| C、1molNa2SO4溶于1L蒸馏水中 |
| D、溶液中含有1molNa+ |
| 142g |
| 142g/mol |
| 142g |
| 142g/mol |
| 1mol |
| 1L |


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
| A、向NaOH溶液中滴加FeCl3饱和溶液 |
| B、向冷水中滴加饱和FeCl3溶液然后加热煮沸 |
| C、向加热煮沸的蒸馏水中逐滴加入少量饱和FeCl3溶液至呈红褐色 |
| D、向饱和的FeCl3溶液中滴加少量的热水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4LH2含有的分子数为NA |
| B、常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA |
| C、通常状况下,1NA个CO2分子占有的体积为22.4L |
| D、1L0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.00 molNaCl中含有6.02×1023个NaCl分子 |
| B、1.00molNaCl中,所有Na+的电子总数为8×6.02×1023 |
| C、电解58.5g 熔融的NaCl,能产生11.2L氯气(标准状况)、23.0g金属钠 |
| D、欲配置1.00L 1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+=2Fe3++3H2O |
| B、氢氧化钡溶液滴入硫酸氢钠溶液至中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| C、亚硫酸钠和足量的稀硝酸混合:SO32-+2H+=SO2↑+H2O |
| D、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2=Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量就是物质的质量 |
| B、摩尔是国际单位制的七个基本物理量之一 |
| C、H2O的摩尔质量为18g |
| D、阿伏加德罗常数的数值约为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属氧化物 氧化铁 FeO |
| B、非金属氧化物 二氧化氮 NO2 |
| C、酸 硫酸 H2SO3 |
| D、碱 纯碱 Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
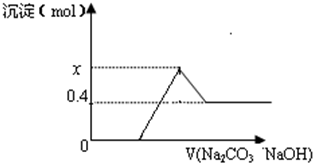 大多金属碳化物能与水剧烈反应,生成相应氢氧化物和气态烃,如:
大多金属碳化物能与水剧烈反应,生成相应氢氧化物和气态烃,如:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com