
【题目】草酸合铁酸钾晶体Kx[Fe(C2O4)y]·3H2O是一种光敏材料,下面是一种制备草酸合铁酸钾晶体的实验流程。
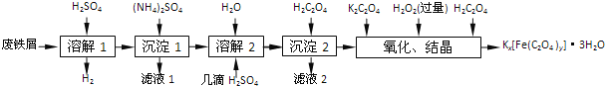
已知:(NH4)2SO4、FeSO4·7H2O、莫尔盐[(NH4)2SO4·FeSO4·6H2O]的溶解度如表:
温度/℃ | 10 | 20 | 30 | 40 | 50 |
(NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
FeSO4·7H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | ― |
(NH4)2SO4·FeSO4·6H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(1)废铁屑在进行“溶解1”前,需用在5% Na2CO3溶液中加热数分钟,并洗涤干净。Na2CO3溶液的作用是________。
(2)“溶解1”应保证铁屑稍过量,其目的是___________。“溶解2”加“几滴H2SO4”的作用是________。
(3)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、________、过滤、用乙醇洗涤、干燥。用乙醇洗涤的目的是____________。
(4)“沉淀”时得到的FeC2O4·2H2O沉淀需用水洗涤干净。检验沉淀是否洗涤干净的方法是_______。
(5)“结晶”应将溶液放在黑暗处等待晶体的析出,这样操作的原因是__________。
(6)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤[备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250 mL待测液。
步骤2:用移液管移取25.00 mL待测液于锥形瓶中,加入稀H2SO4酸化,_________,C2O42-转化为CO2被除去。
步骤3:向步骤2所得溶液中______________。
步骤4:用c mol·L-1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液。
【答案】除油污 防止Fe2+被氧化为Fe3+ 抑制Fe2+水解 冷却结晶 洗去杂质,减少莫尔盐晶体溶解损失,便于快速干燥 用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净 黑暗可以防止晶体分解 加入足量KMnO4溶液 加入稍过量的锌粉,加热至充分反应(溶液黄色刚好消失),过滤、洗涤、将过滤及洗涤所得溶液收集到锥形瓶中
【解析】
废铁屑加入硫酸溶液溶解,加入硫酸铵溶液结晶析出硫酸亚铁晶体,加水溶解,滴入几滴稀硫酸防止亚铁离子水解,加入草酸沉淀亚铁离子,过滤得到沉淀加入重铬酸钾、过氧化氢溶液氧化,最后加入草酸,经过滤得到草酸合铁酸钾晶体。
(1)在5%Na2CO3溶液中加热数分钟,并洗涤干净是利用碳酸钠水解显碱性,油污会发生水解生成溶于水的物质并洗涤除去,作用是去除油污;
(2)Fe2+在空气中易被氧化,“溶解1”应保证铁屑稍过量,其目的是防止Fe2+被氧化为Fe3+;Fe2+在溶液中易水解,则“溶解2”加“几滴H2SO4”的作用抑制Fe2+水解;
(3)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩,冷却结晶,过滤用乙醇洗涤、干燥,防止生成的盐损失,且乙醇易挥发;
(4)取最后一次洗涤液,检查是否含有硫酸根离子进行设计分析,用小试管取少量最后一次洗涤液,加入BaCl2溶液,如出现白色沉淀,说明沉淀没有洗涤干净,否则,沉淀已洗涤干净;
(5)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是黑暗可以防止晶体分解;
(6)步骤1:称量ag三草酸合铁酸钾晶体,配制成250mL溶液;
步骤2:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+;
步骤3:向反应后的溶液中加入适量锌粉使Fe3+全部转化为Fe2+,同时有气泡产生,过滤,洗涤,将过滤及洗涤所得溶液A收集到锥形瓶中,此时,溶液仍呈酸性;
步骤4:用cmol/LKMnO4溶液滴定溶液至终点,消耗KMnO4溶液VmL,反应中MnO4-被还原成Mn2+。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】下列图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。
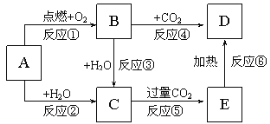
回答下列问题:
(1)写出化学式:A___,D___。
(2)以上反应中不属于氧化还原反应的有___(填序号)。
(3)反应③的离子方程式:___。氧化剂为___;氧化产物为___。
(4)向D溶液中通入CO2反应的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反-2-己烯醛(D)是一种重要的合成香料,下列合成路线是制备D的方法之一。根据该合成路线回答下列问题:
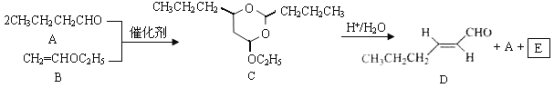
已知: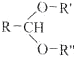
![]() RCHO+R'OH+R"OH
RCHO+R'OH+R"OH
(1)A的名称是__________;B分子中共面原子数目最多为__________;C分子中与环相连的三个基团中,不同化学环境的氢原子共有__________种。
(2)D中含氧官能团的名称是__________,写出检验该官能团的化学反应方程式:__________。
(3)E为有机物,能发生的反应有__________。
a.聚合反应b.加成反应c.消去反应d.取代反应
(4)B的同分异构体F与B有完全相同的官能团,写出F所有可能的结构:________。
(5)以D为主要原料制备己醛(目标化合物),在方框中将合成路线的后半部分补充完整。
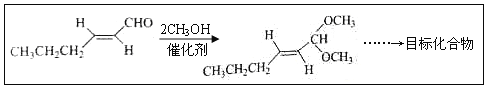
(6)问题(5)的合成路线中第一步反应的目的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空题。
(1)47.5g某二价金属的氯化物中含有1molCl-,则该金属氯化物的摩尔质量为_______ ;该金属的相对原子质量为_______ 。
(2)标准状况下,3.4g NH3 的体积为_______ ;它与标准状况下_______ L H2S含有相同数目的氢原子。
(3)已知CO、CO2混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量为_______ ;CO2在相同状况下的体积为_______ 。
(4)将4g NaOH 溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质 的量浓度为_______。
(5)已知ag氢气中含有b个氢原子,则阿伏加德罗常数的值可表示为 _______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生课外活动小组的同学设计下图所示实验装置,用来验证一氧化碳具有还原性。回答下列问题。
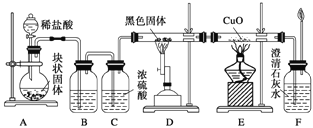
(1)写出装置A中发生反应的化学反应方程式:_______________________。
(2)装置B中最适宜的试剂是:_________________________。
(3)装置D中黑色固体为_____________(填名称),反应的化学方程式为:_____________________________。
(4)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是: ___________________________________。
(5)按照如图装置进行实验时,首先进行的操作名称是_____________。
(6)根据实验中的_________________现象,可证明CO具有还原性,有关反应的化学方程式是___________________________。
(7)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在上图装置________与________之间连接下图中的___________装置(填序号)。
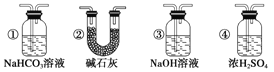
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
盐酸
分子式:HCl
相对分子质量:36.5
密度:1.19g/cm3
质量分数:36.5%
(1)该浓盐酸中HCl的物质的量浓度为______molL-1。
(2)某学生欲用上述浓盐酸和蒸馏水配480mL物质的量浓度为0.200molL-1的稀盐酸。
①配制稀盐酸时,应选用容量瓶的规格是_______mL。
②该学生需要用取___mL上述浓盐酸进行配制。
③若出现如下情况,对所配溶液浓度将有何影响?(填“偏高”、“偏低”或“无影响”)
量取浓盐酸时俯视刻度线_____,定容时仰视刻度线_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和KHSO3能发生反应:ClO3-+HSO3-→SO42-+ Cl-+ H+(未配平)。已知该反应的速率随c(H+)的增大而加快。下图为用ClO3-在单位时间内物质的量浓度变化表示的该反应υ-t图。下列说法正确的
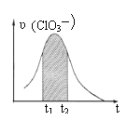
A. 反应开始时速率增大可能是c(H+)所致
B. 纵坐标为υ(Cl-)的υ-t曲线与图中曲线不能完全重合
C. 后期速率υ下降的主要原因是反应向逆反应方向进行
D. 图中阴影“面积”可以表示t1-t2时间内c(SO42-)增加量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组以苯胺为原料,按以下反应原理和流程合成对氨基苯磺酸
![]() +H2SO4
+H2SO4 ![]()
![]() +H2O
+H2O
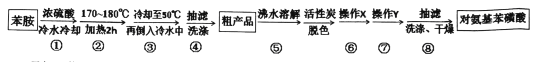
已知:苯胺是一种无色油状液体,微溶于水,易溶于乙醇,熔点-6.1℃,沸点184.4℃。对氨基苯磺酸是一种白色晶体,微溶于冷水,可溶于沸水,易溶于碱性溶液,不溶于乙醇。
(1)下列操作或描述不正确的是________
A.步骤①浓硫酸要分批滴加且不断振荡,并在冰水中冷却目的是为防止苯胺的挥发或碳化
B.步骤③倒入冷水中后,若没有析出晶体,可用玻璃棒搅拌或加入晶种促进晶体析出
C.步骤②加热采用水浴加热,其优点是反应物受热均匀,便于控制温度
D.实验装置中温度计可以改变位置,也可使其水银球浸入在浴液中
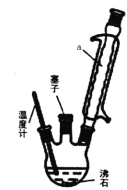
(2)步骤②反应时如图所示装置中进行,其中仪器a的名称_________ 。步骤④中洗涤剂最好选择 ______ 洗涤沉淀的操作是______________。
A. 15%的乙醇 B.热水 C. 冷水 D.NaOH溶液
(3)苯胺与足量浓硫酸反应后,为验证苯胺是否完全反应,可取出几滴反应混合液滴到5-6mL10% NaOH溶液,若 _________现象则认为反应已基本完全。
(4)步骤⑥中操作X为__________,实验有时需要将步骤⑤、⑦、⑧的操作重复多次,其目的是______________________。
(5)苯胺与浓硫酸混合时会反生副反应产生盐类物质,写出其反应化学方程式____。
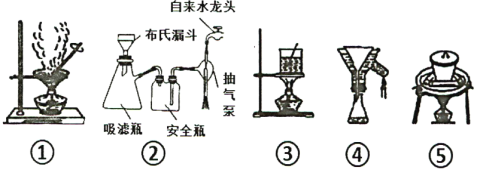
(6)步骤⑤至⑧过程 ,下列装置肯定用不到的是___ ,若制得的晶体颗粒较小,分析可能的原因______(写出两点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于葛根素(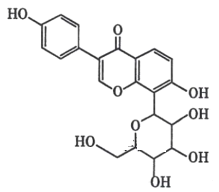 )的说法,正确的是
)的说法,正确的是
A.0.1 mol 葛根素完全燃烧,生成 22.4L(标准状况)H2O
B.1mol 葛根素与溴水反应,最多消耗 2.5mol Br2
C.一定条件下,葛根素能发生氧化、消去及水解等反应
D.与足量 H2 发生加成反应,该分子中官能团的种类减少 2 种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com