
| A、室温下,将pH=2的醋酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
| B、室温下,向pH=3的醋酸溶液加水稀释后,溶液中所有离子浓度均减小 |
| C、向含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| D、向CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
| A、找到了新型高效催化剂 |
| B、充分利用了能量 |
| C、提高了纯碱产品的纯度 |
| D、有效减少了环境污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向无色溶液加入盐酸酸化的氯化钡溶液有白色沉淀,结论:溶液中含有SO42- |
| B、无色溶液焰色反应呈黄色,结论:溶液中含有Na+ |
| C、向无色试液加入硝酸酸化的硝酸银溶液产生白色沉淀,结论:溶液中含Cl-- |
| D、向某溶液中加入氢氧化钠溶液加热,有能使湿润的红色石蕊试纸变蓝的气体生成,结论:溶液中含有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
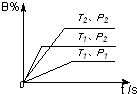 已知某可逆反应m A(g)+n B(气)?p C(气)+Q,在密闭容器中进行,右图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线.由曲线分析,下列判断正确的是( )
已知某可逆反应m A(g)+n B(气)?p C(气)+Q,在密闭容器中进行,右图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线.由曲线分析,下列判断正确的是( )| A、T1<T2,P1>P2,m+n>p,Q>0 |
| B、T1>T2,P1<P2,m+n>p,Q<0 |
| C、T1<T2,P1>P2,m+n<p,Q>0 |
| D、T1>T2,P1<P2,m+n<p,Q>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
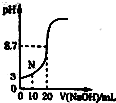 某学习小组用0.10mol?L-1的标准NaOH溶液滴定20.00mL某未知浓度的酸HA,指示剂变色时认为酸碱恰好反应,此时测得溶液的pH为8.7.该小组绘制的滴定曲线如图:
某学习小组用0.10mol?L-1的标准NaOH溶液滴定20.00mL某未知浓度的酸HA,指示剂变色时认为酸碱恰好反应,此时测得溶液的pH为8.7.该小组绘制的滴定曲线如图:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+一定存在 |
| B、100 mL溶液中含0.02 mol CO32- |
| C、Cl-一定存在 |
| D、Ba2+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O2 |
| O2 |
| H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100℃纯水的pH<7,说明升温可导致水呈酸性 |
| B、0.2 mol?L-1的盐酸与等体积水混合后pH=1 |
| C、能自发进行的化学反应,一定是△H<0△S>0 |
| D、Na2CO3溶液中:c(Na+)+c(H+)═c(HCO3-)+c(CO32-)+c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com