
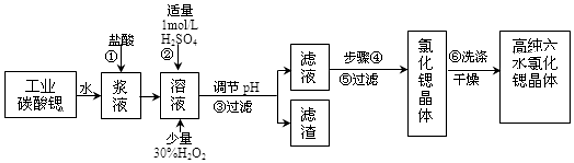
| �������� | Fe��OH��3 | Fe��OH��2 |
| ��ʼ������pH | 1.5 | 6.5 |
| ������ȫ��pH | 3.7 | 9.7 |
���� ��SrCO3Ϊԭ���Ʊ���ˮ�Ȼ��ȣ�SrCl2•6H2O���������̿�֪��SrCO3�����ᷴӦ����Һ�г�����Sr2+��Cl-�⣬����������Fe2+��Ba2+���ʣ�Ȼ��������������ᱵ����������������⣬������ҺpH�����������������������Թ��˺�����Ϊ���ᱵ��������������Һ�к�SrCl2�������������ȴ�ᾧ�õ�SrCl2•6H2O���Դ������
��� �⣺��1��������м���������30%H2O2��Ŀ���ǽ�Fe2+������Fe3+����Ӧ�����ӷ���ʽΪ 2Fe2++H2O2+2H+=2Fe3++2H2O��
�ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O��
��2��������Һ��pHĿ����ʹ�����ӳ�����������Һ��pH��ͬʱ���������������ʣ�����ѡ��SrO��SrCO3��Sr��OH��2�ȣ���Ϊ̼���ȹ����л������������Ļ�������Բ�������������������Ҫ�ɷ���Fe��OH��3��BaSO4��
�ʴ�Ϊ��SrO��SrCO3��Sr��OH��2�ȣ� Fe��OH��3��BaSO4 ��
��3������ܰ�������Ũ������ȴ�ᾧ��Ϊ��ֹ�¶ȹ���ʹ��SrCl2•6H2O ����ʧˮ����˲��� 60�����ˮԡ������������Һ������־�Ĥ��Ȼ����ȴ�ᾧ��A��ȷ���ᾧ����Խ�����õ��ľ������Խ���ý��ͽᾧ���ʵķ������õ��ϴ������SrCl2•6H2O ���壬B��ȷ�� ֻ����Һ�ﵽ�����ͺ��������������ſ��ò���������������Ħ�������ڵķ���ʹ����������C�����������ȴ�ᾧ����˲�����dz��¹��˻��ѹ���ˣ������õ��ߴ�SrCl2•6H2O ���壬����ѡ�����ϴ�Ӽ�Ϊ�����Ȼ�����Һ����С������ܽ�ͬʱҲ��������������ʣ�D����
�ʴ�Ϊ��A��B��
��4��SrCl2•6H2O ������61��ʱ��ʼʧȥ�ᾧˮ���ʹ�ҵ�ϲ��ü�ѹ��ɻ�����50��60����ȷ紵��SrCl2•6H2O���壻
�ʴ�Ϊ����ֹSrCl2•6H2O ������61������ʱʧȥ�ᾧˮ��
��5�����ݹ�ϵʽNH4SCN��AgNO3��֪��������AgNO3������Ϊ0.2 mol/L��0.02 L��170g/mol=0.68g������ݣ�SrCl2•6H2O��2AgNO3
267 2��170
��Ʒ��SrCl2•6H2O������Ϊ��$\frac{267����2.38-0.68��}{2��170}$=1.335g����ԭSrCl2•6H2O����Ĵ���Ϊ$\frac{1.335g}{1.4g}��100%$=95.3%��
�ʴ�Ϊ��95.3%��
���� ���⿼���Ʊ�ʵ�鷽������ƣ�Ϊ��Ƶ���㣬�����Ʊ������з����Ļ�ѧ��Ӧ�����ʷ��뷽��Ϊ���Ĺؼ����漰��Ӧ���ʡ�������ԭ��Ӧ���ζ�ԭ�����ζ�ʵ������ݼ���Ӧ�õȣ�ע����Ϣ����ѧ֪ʶ���ۺ�Ӧ�ã��ۺ��Խ�ǿ����Ŀ�Ѷ��еȣ�


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 200 mL 0.5mol/LNaCl��Һ | B�� | 50 mL 0.3mol/LNa2SO4��Һ | ||
| C�� | 150 mL 0.4mol/LNaOH | D�� | 200mL0.15mol/LNa3PO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʱ�ܶ�֮��Ϊ2��1 | |
| B�� | ԭ�������ʱ���еĵ�����֮��Ϊ1��4 | |
| C�� | �������ʱ���е�������֮��Ϊ4��5 | |
| D�� | ������ʱ���е�ԭ����֮��Ϊ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3�� | B�� | 5�� | C�� | 8�� | D�� | 9�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ԭ�� | ���� |
| A | ��ϩ�ͱ�����ʹ��ˮ��ɫ | �����Ӻ���ϩ���Ӻ�����ͬ��̼̼˫�� |
| B | ��������к����Ȼ� | ����NaHCO3��Һ��Ӧ����CO2 |
| C | ��ά�غ͵��۵Ļ�ѧʽ��Ϊ��C6H10O5��n | ��������ͬ���칹�� |
| D | ������������ϩ��һ�������¶�����ˮ��Ӧ | ��������ͬһ��Ӧ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
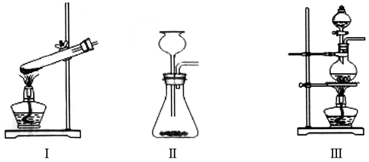
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
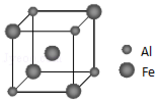
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �þƾ���ȡ��ˮ�еĵ� | |
| B�� | �������к�ˮ���� | |
| C�� | �ù��˵ķ�����ȥNaCl��Һ�к��е��������۽��� | |
| D�� | �ü���-�����ķ������Գ�ȥ�����е�CaCl2��MgCl2������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com