
����Ŀ����������������߲࣬�ԣ�ͼA������ȡ����ʱ����Ϊ߲����߲�����ĸ���ԭ������������ӽ������Ҷ���أ�ͼB���ȶ������ʣ���ش�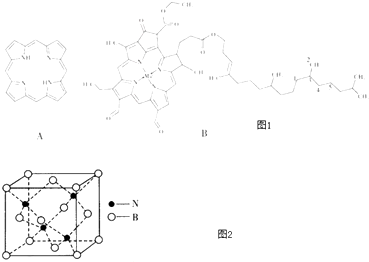
��1��߲����Nԭ�Ӳ��õĹ���ӻ���ʽ��
��2�������й�Ҷ���ط��ӵ�˵����ȷ��������ѡ����ţ���
A.ͼ1��1��5��C����������������
B.�����д�����λ��
C.ͼ1��1��2��3��4��C����
D.N�ĵ�һ�����ܴ���O
��3��߲����Fe2+�ϼ����γ�Ѫ���أ�Fe2+�ĵ����Ų�ʽΪ
��4���軯�⣨HCN����һ�ֺ����綾�����������ЦҼ���м��ĸ�����Ϊ �� �ɷ��ӽṹ�Ʋ⣬�軯������ס����ס�������ˮ��ԭ���� �� �軯���������������CN����ʹ��Ѹ���ж�����ٳ�����CN���ĵȵ����� ��
��5��N��B�ܹ��γ�һ��Ӳ�Ƚӽ����ʯ�����ʣ��侧��ṹ��ͼ2�����侧���߳�Ϊapm�������ܶ�Ϊg��cm��3��ֻ����ʽ����
���𰸡�
��1��sp3��sp2
��2��D
��3��1s22s22p63s23p63d6
��4��1��1���ף�HCN��ˮ���Ǽ��Է��ӣ�������������ԭ��֪��HCN������ˮ��N2��CO
��5��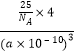
���������⣺��1���۲���ӶԸ�����4��Nԭ�Ӳ���sp3�ӻ����۲���ӶԸ�����3��N����sp2�ӻ������Դ��ǣ�sp3��sp2����2��A������̼ԭ�������ĸ���ͬ��ԭ�ӻ�ԭ���ţ��⼸��̼ԭ��ֻ��3��̼ԭ��������̼ԭ�ӣ��ʴ���B�����йµ��ӶԺͺ��пչ����ԭ��֮�������λ����Nԭ�Ӻ��йµ��Ӷԡ�����ԭ�Ӻ��пչ�������Ժ�����λ��������ȷ��C���ṹ���顢��ϩ�ṹ֪���⼸��̼ԭ��֮�䲻�ܹ��棬�ʴ���D��ͬһ����Ԫ�أ�Ԫ�صĵ�һ����������ԭ��������������������ƣ�����IIA�塢��VA��Ԫ�ص�һ�����ܴ���������Ԫ�أ����Ե縺��N��O������ȷ����ѡBD����3��Fe��26��Ԫ�أ���ԭ�Ӻ�����26�����ӣ�ʧȥ�����������������������ӣ����ݹ���ԭ����д���������Ų�ʽΪ1s22s22p63s23p63d6 �� ���Դ��ǣ�1s22s22p63s23p63d6����4��HCN�ĽṹʽΪH��C��N�����۵���Ϊ�Ҽ������������к���һ���Ҽ������м����÷����к��������Ҽ������м������Զ���֮��Ϊ1��1�����Է��ӵ����ʼ������ڼ��Է��ӵ��ܼ���HCN�Ǽ��Է��ӡ�ˮ�Ǽ��Է��ӣ�����HCN������ˮԭ�Ӹ�����ȡ��۵�������ȵ�����Ϊ�ȵ����壬CN���ĵȵ�������N2��CO�ȣ����Դ��ǣ�1��1���ף�HCN��ˮ���Ǽ��Է��ӣ�������������ԭ��֪��HCN������ˮ��N2��CO����5���þ�����Nԭ�Ӹ���Ϊ4��Bԭ�Ӹ���=8�� ![]() +6��
+6�� ![]() =4���仯ѧʽΪBN���ⳤΪa��10��10cm���������=��a��10��10cm��3 �� �����ܶ�=
=4���仯ѧʽΪBN���ⳤΪa��10��10cm���������=��a��10��10cm��3 �� �����ܶ�= ![]() =
= ![]() =
= 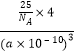 g��cm��3 �� ���Դ��ǣ�
g��cm��3 �� ���Դ��ǣ� 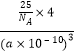 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϸ���ں��������л��������ϸ������ʱ�������Ļ�����ֱ���(����)
A.���κ�����B.ˮ�ͺ���
C.�����ʺ͵�����D.ˮ�͵�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Һ�п��ܴ����ż�ȩ�����в�����֤�����ǣ� ��
A.�������Ƶ�Cu��OH��2���ȣ���ש��ɫ����������֤��һ�����ڼ�ȩ
B.�ܷ���������Ӧ��֤������ȩ
C.��Һ������NaOH��Һ��ϣ����������ɷ���������Ӧ�����м�ȩ
D.�Ƚ���Һ��ֽ���������Ӧ���ռ����������������Ӧ����������������ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧʵ�����������⻯ѧ֪ʶ���γɻ�ѧ������̽���봴��������������ѧ������
��1����ʵ��������Ũ������MnO2������ȡCl2���������ʵ�顣
�� ��ƽ���з���ʽ��
HCl(Ũ) + MnO2 ![]() MnCl2 + Cl2 + H2O___________
MnCl2 + Cl2 + H2O___________
�������ռ�Cl2����ȷװ����_______��
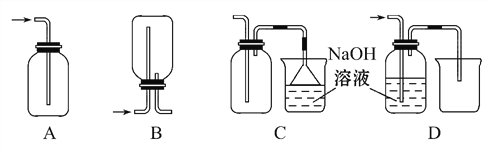
�� ��Cl2ͨ�뵽Ba(OH)2��Һ�з�����Ӧ�Ļ�ѧ����ʽΪ��______
�� ����������ȼ�յĻ�ѧ����ʽΪ��______________
�� ������������ˮ���뵽ʢ������NaHCO3��ĩ���Թ��У��ɿ��������У� ____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��������������ˮ�е�ijЩ�ɷ�(����������)û�й�ϵ����(����)
A. ��Ƭ����������ˮ�У�����ɫ���ݲ���(H��)
B. ������ˮʹ��ɫ������ɫ(HCl)
C. ��������ˮ�еμ�ʯ����Һ����Һ�ȱ�����ɫ(H����HClO)
D. �μ�AgNO3��Һ�а�ɫ��������(Cl��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A��g��+2B��g��C��g��+D��g����H��0��һ���¶��£�2molA��2molB��2L�ܱ������з�Ӧ��10min��ﵽƽ�⣬��ʱ����ѹǿ��Ϊԭ���� ![]() ������������ȷ���ǣ� ��
������������ȷ���ǣ� ��
A.�ӿ�ʼ��ƽ�⣬A�ķ�Ӧ����Ϊ0.08mol?L��1?min��1
B.���ŷ�Ӧ�Ľ��У����������ܶ���С
C.�ﵽƽ��ʱ��B��ת����Ϊ20%
D.���¶��£���Ӧ��ƽ�ⳣ��K= ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��װ�ü������Ի����Ѻõ���( �� )

��ʵ��������(a)װ���ռ����� ��ʵ��������(b)װ�����������Ʒ�Ӧ��ʵ�� ��ʵ�������ò������ֱ�պȡŨ�����Ũ��ˮ���������ᷴӦ������ε�ʵ�� ��ʵ��������(c)װ�ý���ͭ��ϡ����ķ�Ӧ(����)
A. �ڢۢ� B. �٢ڢ� C. �٢ڢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����о�С�飬��ͭ��ͨ����ͬ�Ļ�ѧ��Ӧ��ȡ����������Ƶ�ʵ�����Ϊ��
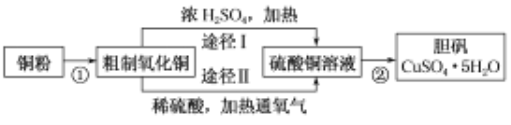
��1���������������յķ���������ʱ�õ���������________(����ĸ)��
a������ ���� b��©�� �� c����Ͳ������ d��������
��2��ͭ�۾����պ�õ��IJ���������ͭ������ͭ�Ļ����ж����к�������ͭ���ķ�����д��ʵ������������ۣ���______________________________________________________________��
��3��;�����е�������ԭ��Ӧ��ѧ����ʽ��_________________________________________________��
��4���ɴ�������ͭͨ������;����ȡ��������;������ȣ�;���������Ե�һ���ŵ���________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��Ԫ�����ڱ���1��20���Ҳ�ͬ����Ԫ����ɵĵ��ʼ�������֮��ת����ϵ�������е�ˮ����ȥ��������AΪ����ɫ���嵥�ʣ���ʵ�����У����ù���B����C������ȡ�̼�����ζ����F��F��G�����Ԫ����ͬ��G��I����������������ͬ����ش�
��1��д��B��I�Ļ�ѧʽB �� I ��
��2����Ӧ�ܵ�ʵ������Ϊ��д��F��һ�־�����; ��
��3�������Ư�����õ�D��Һ����I��Ũ��Һ��A���ɣ��䷴Ӧ�����ӷ���ʽΪ�� ��
��4��д����Ӧ�۵Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com