
| A. | ②中可以采用纯碱溶液,发生的反应是:3Br2+6CO32-+3H2O=5Br-+BrO3-+6HCO3- | |
| B. | 第③步,需加人氧化性酸,才能将Br-氧化为Br2 | |
| C. | B溶液颜色要比A 溶液深 | |
| D. | 第④步,采用的是蒸馏的方法 |
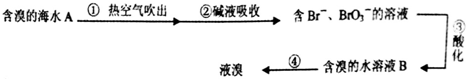
分析 由流程可知,①中发生2Br-+Cl2=2Cl-+Br2,利用空气将吹出塔中含Br2的溶液,经过吹出、吸收、酸化来重新获得含Br2的溶液,其目的是富集溴,提高Br2的浓度,加入碱液重新吸收,所得溶液富含BrO3-,③中发生5Br-+BrO3-+6H+=3Br2+3H2O,最后利用蒸馏得到溴,以此来解答.
解答 解:A.纯碱是碳酸钠,与溴反应有BrO3-生成,反应的离子方程式为3CO32-+3Br2=5Br-+BrO3-+3CO2↑,故A正确;
B.溶液中含有Br-、BrO3-,在酸性条件下可发生发生5Br-+BrO3-+6H+=3Br2+3H2O,无需加入氧化酸,故B错误;
C.B经过富集,浓度较大,则B的颜色比A深,故C正确;
D.溴的浓度较大,与水的沸点不同,可蒸馏分离,故D正确.
故选B.
点评 本题考查海水资源综合利用,涉及了离子的除杂、氧化还原反应、元素及其化合物的有关知识进行综合利用、混合物分离提纯及溴的制备,提高了试题的综合性,为高频考点,把握流程中的反应及物质的性质为解答的关键,侧重分析与实验能力的考查,题目难度中等.


科目:高中化学 来源: 题型:多选题
| A. | CO2气体不能支持任何物质的燃烧 | |
| B. | 铝合金的硬度、熔点比组成合金各成分金属的大 | |
| C. | 将一小块钠放入足量AlCl3溶液中,最终有沉淀生成的 | |
| D. | 常温下,金属镁、铝在空气中都能与氧气反应,所以它们在空气中不能稳定存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在浓氨水中加入生石灰可以制取少量的NH3 | |
| B. | 用水可以一次性鉴别溴苯、苯、乙酸三种物质 | |
| C. | 除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质是H2O、Ba(OH)2、Na2CO3、HCl | |
| D. | 实验室制备乙酸乙酯时,将溶液混合后需用大火迅速加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
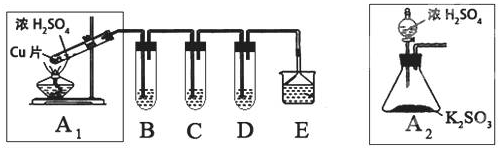
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在SO32-或 SO42-. |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体滴入1滴(或少量)品红,再滴入过量2mol/L盐酸,振荡. | |
| 步骤3:用试管取适量滤液,向其中(或小烧杯中)滴入过量的1mol/LBa(OH)2溶液[或滴入1滴(或少量)品红溶液,再滴入2-3滴(或过量)的2mol/L盐酸],振荡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白色沉淀是CuI2,棕色溶液含有I2 | |
| B. | 滴加KI溶液时,转移1mol电子时生成1mol白色沉淀 | |
| C. | 通入SO2时,SO2与I2反应,I2作还原剂 | |
| D. | 上述实验条件下,物质的氧化性:I2>Cu2+>SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
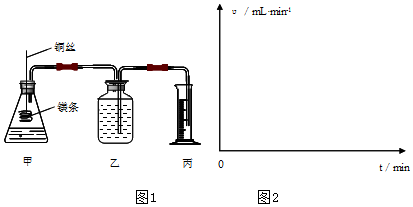
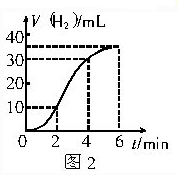
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com