
分析 该烃蒸气密度是相同条件下H2密度的41倍,则其相对分子质量为82,根据含碳量和含氢量,求出分子式,再根据与H2的加成产物是2,2-二甲基丁烷写出结构简式.
解答 解:该烃蒸气的密度是相同条件下H2密度的41倍,则其相对分子量为:2×41=82,分子中含碳87.8%,氢12.2%,则分子中含有C、H原子数分别为:N(C)=$\frac{82×87.8%}{12}$=6、N(H)=$\frac{82×12.2%}{1}$=10,则分子式为:C6H10,该烃与H2的加成产物是2,2-二甲基丁烷,则该烃的结构简式为:C(CH3)3C≡CH;
故答案为:C(CH3)3C≡CH.
点评 本题考查了有机物分子式与结构式的确定,题目难度不大,注意有机物分子式确定中根据含碳量和含氢量的运用,注意抓住题干信息的运用.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯水宜保存在低温、避光条件下 | |
| B. | H2、I2、HI混合气体加压后颜色变深 | |
| C. | SO2催化氧化成SO3的反应,往往加入过量的空气 | |
| D. | 打开汽水瓶,看到有大量的气泡逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 若Z是KCl溶液,则电解时溶液中Cl-向Y极移动 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 外加电流的阴极保护法中,Y是待保护金属 | |
| D. | 电解硫酸溶液一段时间后,加适量水可使溶液恢复到原溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 现有五种物质A、B、C、D、E,分别是稀盐酸、氢氧化钠溶液、铁、碳、二氧化碳中的某一种,D属于酸性氧化物,五种物质间的关系如图,相交叉物质间能发生反应,不相交叉物质间不能发生反应.请回答下列问题:
现有五种物质A、B、C、D、E,分别是稀盐酸、氢氧化钠溶液、铁、碳、二氧化碳中的某一种,D属于酸性氧化物,五种物质间的关系如图,相交叉物质间能发生反应,不相交叉物质间不能发生反应.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
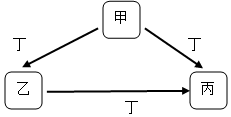 甲、乙、丙、丁均为中学化学常见物质,一定条件下它们有如下转化关系(其它产物已略去).
甲、乙、丙、丁均为中学化学常见物质,一定条件下它们有如下转化关系(其它产物已略去).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
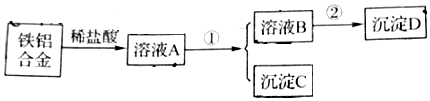
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com