
| A”¢±ź×¼×“æöĻĀ£¬22.4L±½ŗ¬ÓŠNAøö±½·Ö×Ó | B”¢0.2mol?L-1 FeCl3ČÜŅŗÖŠŗ¬ÓŠCl-×ÜŹżĪŖ0.6NA | C”¢ŌŚ±ź×¼×“æöĻĀ£¬ŗ¬4molHClµÄÅØŃĪĖįÓė×ćĮæµÄMnO2·“Ó¦æÉÉś³É22.4LĀČĘų | D”¢4gŗ¤ĘųĖłŗ¬·Ö×ÓŹżĪŖNA |


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| øßĪĀ |
| “߻ƼĮ |
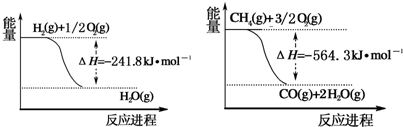
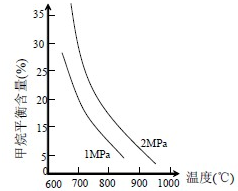
| n(H2O) |
| n(CH4) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ĪļÖŹµÄĮæŹĒČĖĆĒÖ÷¹Ū¹ę¶ØµÄ»ł±¾ĪļĄķĮæÖ®Ņ» | B”¢ĪļÖŹµÄĮæŹµÖŹÉĻ¾ĶŹĒĪļÖŹµÄÖŹĮæ | C”¢ĪļÖŹµÄĮæŹĒČĖĆĒøł¾ŻĘäĖūµÄĪļĄķĮæĶʵ¼³öĄ“µÄŠĀµÄĪļĄķĮæ | D”¢ĪļÖŹµÄĮæŹĒŅ»ÖÖĪļĄķĮæµÄµ„Ī» |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢±ź×¼×“æö£¬1mol SO3ŗ¬OŌ×ÓøöŹżĪŖ3NA | B”¢1.12L N2ÖŠŗ¬N2·Ö×ÓŹżĪŖ0.05NA | C”¢5.6g FeÓė×ćĮæĻ”ŃĪĖį·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.3NA | D”¢³£ĪĀĻĀpH=1µÄH2SO4ČÜŅŗÖŠ£¬H+µÄÅضČĪŖ0.20mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢pH=1µÄĻ”ĮņĖįÖŠŗ¬ÓŠµÄH+ŹżĪŖ0.1NA | B”¢78g±½ŗ¬ÓŠCØTCĖ«¼üµÄŹżÄæĪŖ3NA | C”¢³£ĪĀĻĀ£¬20L pH=12µÄNa2CO3ČÜŅŗÖŠŗ¬ÓŠµÄOH-Ąė×ÓŹżĪŖ0.2NA | D”¢±ź×¼×“æöĻĀ£¬6.72L NO2ÓėĖ®³ä·Ö·“Ó¦×ŖŅʵĵē×ÓŹżÄæĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ÓŠ2.7g Al²Ī¼Ó·“Ó¦ŗó£¬ČÜŅŗÖŠAlO2-ŹżÄæĪŖ0.1NA | B”¢ĆæÉś³É0.6mol H2£¬±»»¹ŌµÄĖ®·Ö×ÓŹżÄæĪŖ1.2NA | C”¢ÓŠ6.72L H2Éś³ÉŹ±£¬·“Ó¦ÖŠ×ŖŅʵĵē×ÓŹżÄæĪŖ0.6NA | D”¢ČÜŅŗÖŠĆæŌö¼Ó0.1mol AlO2-£¬Na+µÄŹżÄæ¾ĶŌö¼Ó0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢1mol C7H16ÖŠŗ¬ÓŠ23NA¹²ÓƵē×Ó¶Ō | B”¢±ź×¼×“æöĻĀ£¬1.12L NH3ÖŠŗ¬ÓŠ0.5NAµē×Ó | C”¢1mol FeÓė×ćĮæH2O£Øg£©·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ2NA | D”¢0.1mol?L-1µÄNaHSO4ČÜŅŗÖŠŗ¬ÓŠŃōĄė×ÓµÄĪļÖŹµÄĮæĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢9g 18O2ŗ¬ÓŠµÄÖŠ×ÓŹżĪŖ5NA | B”¢±ź×¼×“æöĻĀ£¬0.5NA Br2ĖłÕ¼µÄĢå»żŌ¼ĪŖ11.2L | C”¢³£ĪĀĻĀ£¬1L 0.1mol?L-1 NH4NO3ČÜŅŗÖŠŗ¬ÓŠµÄNH4+ŹżĪŖ0.1NA | D”¢Ņ»¶ØĢõ¼žĻĀ£¬1mol N2ŗĶ3mol H2ŌŚĆܱÕČŻĘ÷³ä·Ö·“Ó¦£¬Éś³ÉN-H¼üµÄŹżÄæĪŖ6NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014~2015ѧğÖŲĒģŹŠ9ŌĀŌĀæ¼øßŅ»»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØŗĻĄķµÄŹĒ
A£®ČōX+ ŗĶY2 - µÄŗĖĶāµē×Ó²ć½į¹¹ĻąĶ¬£¬ŌņŌ×ÓŠņŹż£ŗX>Y
B£®ÓÉĖ®ČÜŅŗµÄĖįŠŌ£ŗHCI>H2S£¬æÉĶʶĻ³öŌŖĖŲµÄ·Ē½šŹōŠŌ£ŗCl>S
C£®ĮŚōĒ»ł±½¼×Č©·ŠµćøßÓŚ¶ŌōĒ»ł±½¼×Č©ŹĒŅņĪŖŠĪ³ÉĮĖ·Ö×ÓÄŚĒā¼ü
D£®H”ŖF”¢H”ŖO”¢H”ŖNČżÖÖ¹²¼Ū¼üµÄ¼«ŠŌÖš½„ŌöĒæ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com