
实验室合成乙酸乙酯的步骤如下:在园底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
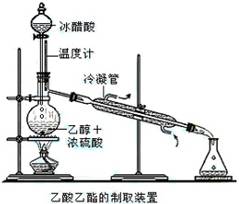
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入几块碎瓷片,其目的是________
(2)在烧瓶中加入一定比例的乙醇和浓硫酸的混合液的方法是:
(3)在该实验中,若用1mol乙醇和1mol 乙酸在浓硫酸作用下加热,充分反应,能否生成1mol乙酸乙酯? ,原因是
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。图中圆括号内为适当的试剂,方括号内为适当的分离方法。(提示:A为乙酸乙酯,E为乙醇)
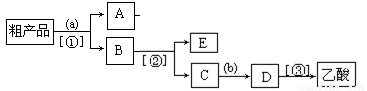
试剂a是__________,分离方法①是_________________,分离方法②是___________
(1)防止暴沸
(2)先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡
(3)否、该反应是可逆反应,反应不能进行到底
(4)饱和碳酸钠溶液、分液、蒸馏
【解析】考查乙酸乙酯的制备。
(1)实验室制取乙酸乙酯需要加热,所以为防止液体暴沸,需要加入碎瓷片,防止暴沸。
(2)浓硫酸的密度大于水,且浓硫酸稀释会放出大量的热,所以正确的方法是先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡。
(3)酯化反应是可逆反应,所以1mol乙酸和1mol乙醇不可能生成1mol乙酸乙酯。
(4)制取的乙酸乙酯中含有乙酸和乙醇,所以要提取乙酸乙酯,可以利用乙酸乙酯难溶于水进行分离。先加入饱和碳酸钠溶液,来溶解乙醇,吸收乙酸,分液即得到乙酸乙酯(即A),乙醇和乙酸钠的混合液(即B)。乙醇的沸点较低,蒸馏即得到乙醇,因此E是乙醇,C是乙酸钠的混合液。向乙酸钠中加入硫酸,生成乙酸(即D),最后蒸馏即得到乙酸。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
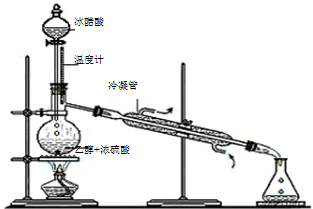
 实验室合成乙酸乙酯的步骤如下:在园底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
实验室合成乙酸乙酯的步骤如下:在园底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 有机化学知识在生活中应用广泛.
有机化学知识在生活中应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
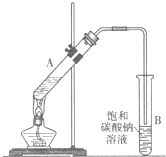 乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.
乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.| 乙酸 | 乙醇 | 乙酸乙酯 | 乙醚 | |
| 沸点/℃ | 118 | 78.3 | 77.1 | 34.5 |
| 溶解性 | 易溶于水 | 极易溶于水 | 与乙醚混溶 | 微溶于水 |
| 浓硫酸 |
| ℃140 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com