
| A. | 利用聚光手电筒照射,可以区别溶液和胶体 | |
| B. | 溶液、胶体、悬浊液和乳浊液等分散系中的溶质均以分子形式存在 | |
| C. | 分散质粒子的直径在1×10-9~1×10-7m之间的分散系属于胶体 | |
| D. | 自来水厂常用某些铁盐或铝盐作净水剂 |
分析 A.胶体具有丁达尔效应;
B.溶液中分散质可以为分子、离子等;
C.胶体区别于其它分散系的本质特征是胶体粒子直径在1-100nm(10-7~10-9m)之间;
D.铝离子、铁离子水溶液中水解生成氢氧化铝、氢氧化铁胶体具有吸附悬浮杂质的作用.
解答 解:A.胶体具有丁达尔效应,可以用来区别胶体与溶液,故A正确;
B.溶液中分散质可以为分子、离子等,故B错误;
C.分散质粒子的直径在1×10-9~1×10-7m之间的分散系属于胶体,故C正确;
D.铝离子、铁离子水溶液中水解生成氢氧化铝、氢氧化铁胶体具有吸附悬浮杂质的作用,能够净水,故D正确;
故选:B.
点评 本题考查了胶体的性质及用途,熟悉胶体分散系本质特征及性质是解题关键,题目难度不大.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:实验题
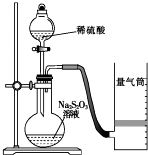 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
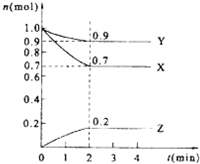 某温度时,在5L的密闭容器中,X、Y、Z的物质的量随时间的变化曲线如图所示.
某温度时,在5L的密闭容器中,X、Y、Z的物质的量随时间的变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+ Na+SO42- Cl- | B. | Cu2+ Al3+ Cl-SO42- | ||
| C. | Fe2+NO3-Cl-CO32- | D. | Ag+ Na+NO3- Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com