
【题目】某学生做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关实验现象.现在请你帮助该学生整理并完成实验报告.
(1)实验目的: ______
(2)实验用品:药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳.
仪器:① ______ ;② ______ ![]() 请填写两件主要的玻璃仪器
请填写两件主要的玻璃仪器![]()
(3)实验内容:
序号 | 实验方案 | 实验现象 |
① | 将少量氯水滴入盛有少量NaBr溶液的试管中,振荡;再滴入少量四氯化碳,振荡 | 加入氯水后,溶液由无色变为橙色,滴入四氯化碳后,水层颜色变浅,四氯化碳层 |
② | 将少量溴水滴入盛有少量KI溶液的试管中,振荡;再滴入少量四氯化碳,振荡 | 加入溴水后,溶液由无色变为黄色,滴入四氯化碳后,水层颜色变浅,四氯化碳层 |
(4)实验结论: ______ .
(5)问题和讨论:请用结构理论简单说明得出上述结论的原因. ______ .
【答案】探究同一主族元素性质的递变规律 试管 胶头滴管 同一主族元素,自上而下,元素的非金属性依次减弱 同一主族元素,自上而下,元素原子的电子层数增多,原子半径增大,原子核对最外层电子的吸引力逐渐减弱
【解析】
氯气具有氧化性,能将溴离子氧化为溴单质,溴单质在有机层显示橙红色;溴单质能将碘离子氧化为碘单质,碘单质在有机层中显示紫红色,结合原子结构与元素性质的关系分析解答。
(1)根据实验现象结合氧化剂的氧化性强于氧化产物的氧化性来得出同主族元素性质的递变规律,故答案为:探究同一主族元素性质的递变规律;
(2)根据实验步骤,实验在试管内进行,再滴入少量四氯化碳,振荡,滴加液体用胶头滴管,故答案为:试管;胶头滴管;
(4)氯气能将溴离子从其水溶液中置换出来,而溴单质能将碘离子从其水溶液中置换出来,说明氧化性是氯气强于溴单质,溴单质强于碘单质,元素的非金属性越强,即非金属性:Cl>Br>I,得出同主族元素性质的递变规律:同主族元素性质相似,且从上到下,元素的非金属性逐渐减弱,故答案为:同一主族元素,自上而下,元素的非金属性依次减弱;
(5)依据原子理论解释为:同一主族元素,自上而下,随原子序数的增加,原子半径逐渐增大,原子核对于核外电子的引力渐强,原子失电子能力减弱,故答案为:同一主族元素,自上而下,元素原子的电子层数增多,原子半径增大,原子核对最外层电子的吸引力逐渐减弱。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)用A质子数,B中子数,C核外电子数,D最外层电子数,用序号回答下列问题。
①原子种类由______决定;
②元素种类由______决定;
③元素的化合价由______决定。
(2)2.0g由![]() 和
和![]() 构成的水
构成的水![]() ,该水分子的物质的量为______,含中子数为______。
,该水分子的物质的量为______,含中子数为______。
(3)核内中子数为N的![]() ,质量数为A,则该离子的核外电子数为______。
,质量数为A,则该离子的核外电子数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有MgCl2和Al2(SO4)3的混合溶液,向其中逐滴加入NaOH溶液,得到沉淀的物质的量与加入NaOH的物质的量关系如图所示,则原溶液中Cl-与SO42-的物质的量之比为( )

A.4∶3B.1∶3C.1∶4D.2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“![]() ”或“
”或“![]() ”回答下列问题
”回答下列问题
①元素的非金属性越强,其对应最高价氧化物水化物的酸性越______;
②元素的金属性越强,其对应最高价氧化物水化物的碱性越______;
③元素的______性越强,其对应气态氢化物的稳定性越______;
④酸性:![]() ______
______![]() ;气态氢化物稳定性:
;气态氢化物稳定性:![]() ______HCl。
______HCl。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选相应实验目的填入下述括号内:
A、验证同主族元素的金属性从上至下递增
B、验证同主族元素的非金属性从上至下递减
C、验证同周期元素的金属性从左至右递减
D、验证同周期元素的非金属性从左至右递增
实验1、比较钠、镁、铝分别与水反应的快慢 ______
实验2、溴化钠溶液中滴入氯水,碘化钠溶液中滴入溴水 ______
实验3、比较钾、钠分别与水反应的快慢 ______
实验4、在![]() 、
、![]() 溶液中逐滴加入NaOH溶液至过量,从而比较
溶液中逐滴加入NaOH溶液至过量,从而比较![]() 、
、![]() 的碱性 ______ .
的碱性 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯是一种重要的有机化工原料,用于制丙烯腈、环氧丙烷、丙酮等。回答下列问题:
(1)已知:
I.C3H8(g)![]() C3H6(g)+H2(g) △H1=+124kJ/mol
C3H6(g)+H2(g) △H1=+124kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=-484kJ/mol
则丙烷氧化脱氢制丙烯反应2C3H8(g)+O2(g)![]() 2C3H6(g)+2H2O(g)的△H为_________kJ/mol。
2C3H6(g)+2H2O(g)的△H为_________kJ/mol。
(2)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程如图所示,其中吸附在催化剂表面的物种用*标注。
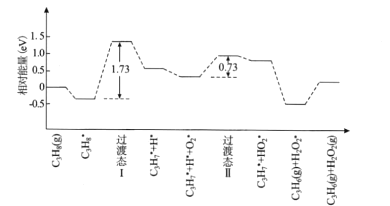
①该反应历程中决速步骤的能垒(活化能)为_________eV,该步骤的化学方程式为________
②请补充该历程之后可能发生的化学反应方程式_____________
(3)已知丙烷氧化脱氢容易发生副反应:2C3H8(g)+O2(g)![]() 3C2H4(g)+2H2O(g)如图所示是丙烷氧化脱氢制丙烯反应达到平衡时丙烷转化率与丙烯选择性随温度变化的曲线[丙烯的选择性=n=
3C2H4(g)+2H2O(g)如图所示是丙烷氧化脱氢制丙烯反应达到平衡时丙烷转化率与丙烯选择性随温度变化的曲线[丙烯的选择性=n=![]() ×100%]
×100%]
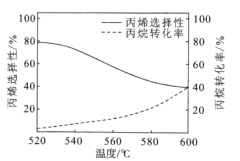
①丙烯的选择性随着温度的升高而降低的可能原因有_________
②在反应温度为600℃,将C3H8与O2以体积比为1:1充入刚性容器中,达到平衡时,丙烷的转化率为40%,丙烯的选择性也为40%,体系总压强为pkPa,则氧气的转化率![]() (O2)=______________丙烯的分压p(C3H8)=____________(结果保留2位有效数字)。
(O2)=______________丙烯的分压p(C3H8)=____________(结果保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,卤化银(AgX,X=Cl,Br)的2条溶解平衡曲线如图所示,已知AgCl,AgBr的Ksp依次减小,且p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-),利用pX-pAg的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系.下列说法错误的是
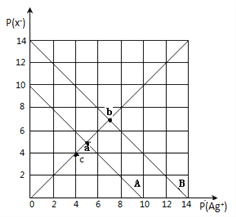
A. t℃时,c点可表示AgCl的不饱和溶液
B. B线表示的是AgBr
C. 取a、b两点处溶液等体积混合,维持t℃不变,混合溶液中一定无白色沉淀生成
D. 在t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K≈104
AgBr(s)+Cl-(aq)平衡常数K≈104
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解NaB(OH)4溶液制备H3BO3的原理如下图所示,下列叙述错误的是
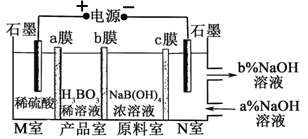
A. M室发生的电极反应式:2H2O-4e-=O2↑+4H+
B. a、c为阴离子交换膜,b为阳离子交换膜
C. N室中:a%<b%
D. 理论上每生成1 mol H3BO3,两极室共产生标准状况下16.8 L气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com