
A、由乙二醇制取高分子 是通过加聚反应完成的 是通过加聚反应完成的 |
| B、乙醇在浓硫酸作催化剂,并且加热的条件下一定发生消去反应 |
| C、卤代烃一般来说在NaOH的水溶液中能发生取代反应,而在NaOH的醇溶液中不一定能发生消去反应 |
| D、酯类物质在一定条件下水解一定得到相应的羧酸和醇 |


科目:高中化学 来源: 题型:
| A、18.4mol/L |
| B、9.2mol/L |
| C、13mol/L |
| D、12mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、电池的负极反应式为:ClO-+H2O+2e-═Cl-+2OH- |
| B、当有0.1 mol Al完全溶解时,流经电解液的电子数为1.806×1023个 |
| C、往滤纸上滴加酚酞试液,b极附近颜色变红 |
| D、b极附近会生成蓝色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、K+、Fe2+、NO3- |
| B、OH-、Cl-、Na+、Mg2+ |
| C、Al3+、K+、Cl-、NO3- |
| D、Cu2+、NO3-、OH-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO (g) 十H2O (g)?CO2(g) 十 H2 (g);△H<0
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO (g) 十H2O (g)?CO2(g) 十 H2 (g);△H<0| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化学 来源: 题型:
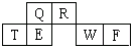 短周期元素Q、R、T、E、W、F在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,T元素为地壳中含量最多的金属元素.
短周期元素Q、R、T、E、W、F在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,T元素为地壳中含量最多的金属元素.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com