
【题目】合成氨工业中,原料气(N2、H2及CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(l)溶液来吸收原料中的CO,其反应是
[Cu(NH3)2Ac]+CO+NH3![]() [Cu(NH3)3]Ac·CO+Q
[Cu(NH3)3]Ac·CO+Q
(1)必须除去原料气中CO的原因是?
(2)醋酸二氨合铜(l)吸收CO的适宜条件是。
(3)吸收CO后的醋酸铜氨液经过适当处理又可再生,恢复其吸收CO的能力以循环使用,醋酸铜氨液再生的适宜条件是。
【答案】
(1)
CO可引起催化剂中毒
(2)低温、高压
(3)高温、低压
【解析】(1)CO可引起催化剂(铁触媒)的中毒,故要除去。(2)题给信息方程式是一个气体体积减小的放热反应,为使醋酸二氨合铜(l)更好的吸收CO,即平衡向正反应方向移动,适宜条件应是低温、高压。(3)醋酸铜氨液再生,即平衡向逆反应方向移动,适宜的条件应是高温、低压。
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)),还要掌握化学平衡移动原理以及影响因素(影响因素:①浓度:增大反应物(或减小生成物)浓度,平衡向正反应方向移动;②压强:增大压强平衡向气体体积减小的方向移动.减小压强平衡向气体体积增大的方向移动;③温度:升高温度,平衡向吸热反应方向移动.降低温度,平衡向放热反应方向移动;④催化剂:不能影响平衡移动)的相关知识才是答题的关键.


科目:高中化学 来源: 题型:
【题目】对比甲烷和乙烯的燃烧反应,下列叙述中正确的是( )
A. 二者燃烧时现象完全相同
B. 点燃前都不用验纯
C. 甲烷燃烧的火焰呈淡蓝色,乙烯燃烧的火焰较明亮
D. 二者燃烧时都有黑烟生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的提纯或离子检验的方法正确的是
A.用渗析的方法精制氢氧化铁胶体
B.以精铜为阳极,粗铜为阴极,CuSO4溶液为电解液精炼铜
C.除去KCl溶液中的少量MgCl2,加入过量KOH溶液,然后过滤即可
D.加入澄清石灰水,能产生白色沉淀,则原溶液中一定含有CO32—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g) ![]() 2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
A.点a的正反应速率比点b的小
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773 K下反应至t1时刻,n(H2)比上图中d点的值大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL混合液中,HNO3和H2SO4的物质的量浓度分别为0.4mol/L和0.1mol/L.向该混合液中加入1.92g铜粉,加热使反应发生完全.下列说法正确的是(忽略反应前后溶液体积变化)( )
A.所得溶液中c(Cu2+)=0.225mol/L
B.所得溶液中c(Cu2+)=0.03mol/L
C.所得气体在标准状况下的体积为0.448L
D.反应中转移0.06mol的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究外界条件对过氧化氢分解速率的影响,某化学兴趣小组的同学做了以下实验.
编号 | 实验操作 | 实验现象 |
① | 分别在试管A、B中加入5mL5%H2O2溶液,各滴入3滴 | 试管A中不再产生气泡; |
② | 另取两支试管分别加入5mL5%H2O2溶液和5mL10%H2O2 | 两支试管中均未明显见到有 |
请回答下列问题:
(1)过氧化氢分解的化学方程式为 .
(2)实验①的目的是 .
(3)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,你提出的对上述操作的改进意见是(用实验中所提供的几种试剂).
(4)某同学在50mL一定浓度的H2O2溶液中加入适量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图1所示,则A,B,C三点所表示的瞬时反应速率最慢的是(填字母代号). 
(5)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,该兴趣化学小组的同学分别设计了如图2、3所示的实验.请回答相关问题: 
①定性分析:如图2可通过观 , 定性比较得出结论;该实验中将FeCl3溶液改为Fe2(SO4)3溶液的原因是 .
②定量分析:用图3所示装置做对照试验,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略.实验中需要测量的数据是 .
(6)通过对上述实验过程的分析,在实验设计时,要考虑方法的应用.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.
(1)一定温度下,向固定体积为2L的密闭容器中充入SO2和NO2各1mol,发生反应SO2(g)+NO2(g)SO3(g)+NO(g),测得上述反应5min末到达平衡,此时容器中NO与NO2的体积比为3:1,则这段时间内SO2的反应速率υ(SO2)= , 此反应在该温度下的平衡常数K= .
(2)甲醇日趋成为重要的有机燃料,通常利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示: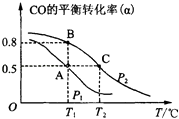
①上述合成甲醇的反应为反应(填“放热”或“吸热”).
②A、B、C三点的平衡常数KA、KB、KC的大小关系为 . A、B两点对应的压强大小关系是PAPB(填“大于”、“小于”或“等于”).
③若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为 , 理论上通过外电路的电子最多为 mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图1: 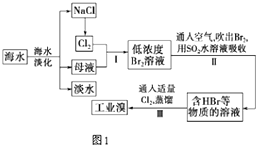
(1)请列举海水淡化的两种方法:、 .
(2)步骤I中己获得Br2 , 步骤II中又将Br2还原为Br﹣ . 其目的是 .
(3)步骤II用SO2水溶液吸收Br2 , 吸收率可达95%.有关反应的离子方程式为 .
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法.查阅了有关资料知:Br2的沸点为59℃.微溶于水,有毒并有强腐蚀性.他们参观生产过程后.画了如图2装置简图: 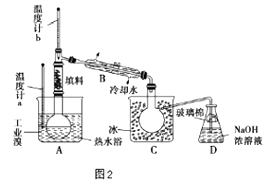
请你参与分析讨论:
①图中仪器B的名称是 .
②整套实验装皿中仪器连接均不能用橡胶塞和橡胶管.其原因是 .
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件? .
④C中液体颜色为 . 为除去该产物中仍残留的少量Cl2 , 可向其中加入NaBr,溶液,充分反应后.再进行的分离操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甘蔗是我们生活中较为常见的经济作物. 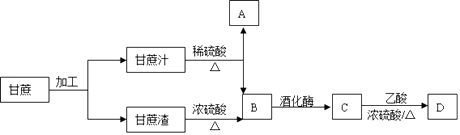
(1)B的分子式是 .
(2)向试管中加入甘蔗渣经浓硫酸水解后的混合液,先加NaOH溶液,再加新制氢氧化铜,加热,可看到(现象).
(3)写出C→D的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com