
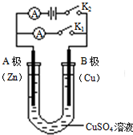
 如右图所示,请按要求回答下列问题.
如右图所示,请按要求回答下列问题.分析 (1)若打开K2,合并K1,形成原电池反应,A极Zn为负极,被氧化,B极Cu为正极,发生还原反应生成铜;
(2)若打开K1,合并K2,为电解池,B为阳极,A为阴极,该极上析出金属铜,根据电子守恒进行计算.
解答 解:(1)若打开K2,合并K1,形成原电池反应,A极Zn为负极,锌不断溶解,Zn-2e-=Zn2+,B极Cu为正极,发生还原反应生成铜,电极方程式为Cu2++2e-═Cu,有红色物质析出,
故答案为:负; A处金属不断溶解;Cu2++2e-=Cu;
②若打开K1,合并K2,为电解池,B为阳极,反应为Cu-2e-=Cu2+;A为阴极,该极上析出金属铜,发生Cu2++2e-═Cu,所以当有0.2mol电子转移时,则析出铜的质量为6.4g,故答案为:阴;A上有红色金属析出;Cu-2e-=Cu2+;6.4.
点评 本题考查了原电池和电解池原理,知道原电池和电解池区别,知道各个电极上发生的电极反应,再结合各个物理量之间的关系式计算,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 平衡常数减小 | B. | CaO 的量不变 | C. | CO2浓度不变 | D. | CO2 浓度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Na+、SO42-、Br- | B. | Na+、NH4+、NO3-、I- | ||
| C. | K+、Mg2+、Fe3+、Cl- | D. | Na+、AlO2-、SO42-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯与丁烯 | B. | 丙烷与丁炔 | C. | 乙烯与乙炔 | D. | 乙烷与丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.4mol/L | B. | 0.2mol/L | C. | 0.1mol/L | D. | 0.08mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com