
下列离子方程式正确的是
A.等物质的量的Ba(OH)2与明矾[KAl(SO4)2·12H2O]加入足量水中:
3Ba2++6OH-+2Al3++3SO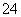 ===3BaSO4↓+2Al(OH)3↓
===3BaSO4↓+2Al(OH)3↓
B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+===Fe3++3H2O
C.H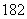 O中投入Na2O2固体:2H
O中投入Na2O2固体:2H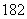 O+2Na2O2===4OH-+4Na++18O2↑
O+2Na2O2===4OH-+4Na++18O2↑
D.CuCl2溶液中加入H2S溶液:Cu2++S2-===CuS↓
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
将相同质量的镁条分别在①O2,②N2,③空气,④CO2中完全燃烧,燃烧后所得固体产物的质量由小到大的顺序是( )
A.②<①<③<④ B.①=②=③=④
C.②<③<①<④ D.②<③<①=④
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法一定正确的是 ( )
A.常温下,1 L 0.1 mol/L的NH4NO3溶液中氧原子数为0.3NA
B.1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA
C.常温、常压下,4.6 g NO2和N2O4混合气体中含有的O原子数目为0.2NA
D.Fe与水蒸气在高温条件下反应,有1 mol Fe参与反应,则转移电子的数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
两种大气污染物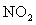 和
和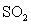 在一定条件下可发生如下反
在一定条件下可发生如下反
应:NO2 + SO2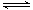 NO + SO3,在体积为VL的密闭容器中通入
NO + SO3,在体积为VL的密闭容器中通入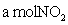 和
和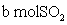 ,反应后容器内硫原子和氧原子的个数比为( )
,反应后容器内硫原子和氧原子的个数比为( )
A.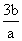 B.
B.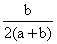 C.
C.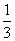 D.
D.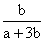
查看答案和解析>>
科目:高中化学 来源: 题型:
为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验Ⅰ:反应产物的定性探究。
实验装置如图所示:(固定装置已略去)

(1)A中反应的化学方程式为 。
(2)F烧杯中的溶液通常是 。
(3)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是
。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
(5)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。实验方案为 。
实验Ⅱ:反应产物的定量探究
(6)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
资料1:
| 硫酸/mol·L-1 | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
资料2:X-射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种。仅由上述资料可得出的正确结论是 __。
a.铜与浓硫酸反应时所涉及的反应可能不止一个
b.硫酸浓度选择适当,可避免最后产物中出现黑色物质
c.该反应发生的条件之一是硫酸浓度≥15 mol/L
d.硫酸浓度越大,黑色物质越快出现、越难消失
(7)为测出硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00 mL加入足量KI溶液振荡,以淀粉溶液为指示剂,用b mol/L Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液V mL。若反应消耗铜的质量为a g,则硫酸铜的产率为 _。(已知:2Cu2++4I-===2CuI+I2,2S2O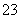 +I2===S4O
+I2===S4O +2I-)
+2I-)
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、NH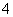 、Mg2+、Fe3+、Al3+、
、Mg2+、Fe3+、Al3+、
SO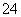 、HCO
、HCO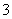 等离子中的一种或几种。当向该溶液中加入一定物质的量的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如下图所示。
等离子中的一种或几种。当向该溶液中加入一定物质的量的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如下图所示。
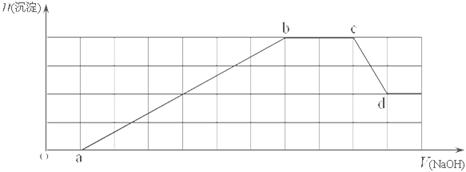
(1)原溶液中一定含有 ,一定不含有 ;
(2)cd段发生的离子反应为 ;
(3)原溶液中物质的量浓度最大的阳离子与原溶液中的阴离子的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定质量的铁、氧化铁、氧化铜的混
合物粉末放入100mL 4.40 mol/L盐酸中,充分反应后产生896 mL H2(标准状况),残留固体1.28g。过滤,滤液中无Cu2+。将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L。则原混合物中单质铁的质量是
A.2.24g B.3.36g C.5.60g D.10.08g
查看答案和解析>>
科目:高中化学 来源: 题型:
在浓盐酸中H3AsO3与SnCl2的离子方程式为:3SnCl2+12Cl-+6 H++2H3AsO3=== 2As +3SnCl62-+6M,关于该反应的说法中正确的组合是
①氧化剂是H3AsO3 ②还原性:Cl->As ③ 每生成1mol As,反应中转移电子的物质的量为3 mol ④ M为OH- ⑤ SnCl62-是氧化产物
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于实验室制取气体所用试剂的组合中,不合理的是( )
A.制Cl2:MnO2、盐酸(浓) B.制H2:硫酸(稀)、Zn
C.制O2:MnO2、H2O2 D.制CO2:硫酸(稀)、CaCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com